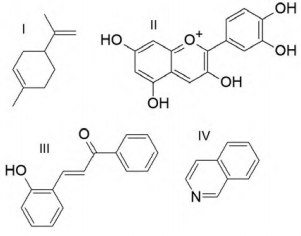
A melanina apresenta o seguinte monômero:

Leia o texto a seguir:
Melanina é uma proteína que confere pigmentação à pele e aos cabelos dos mamíferos. Algumas pessoas
são albinas, pois em seu organismo não existe a produção de melanina.
A melanina é responsável pela cor da pele, dos olhos, dos pelos humanos e atua também em outros
animais. Porém, a cor da pele não depende apenas dos pigmentos da melanina, também do caroteno, que se
localiza no tecido adiposo subcutâneo, que tem a cor alaranjada. Além da melanina e do caroteno, os vasos
sanguíneos também influenciam na cor da pele, pois quanto mais ligeiros e dilatados, mais a pele fica escura.
Quanto mais melanina a pessoa tiver em seu corpo, mais escura será a pele. Quanto menos melanina, mais
clara a pele será.
A melanina é considerada uma proteína. Ela é produzida pelas células que se localizam na camada basal
da epiderme, denominadas de melanoblastos.
Fonte: HTTP://www.mundoeducacao.com.br/biologia/melanina.htm
As funções químicas presentes no monômero da melanina são: