Um grupo de pesquisadoras testava o efeito inibitório
de extratos de um produto natural sobre a atividade de certa enzima envolvida em uma doença. A equipe preparou
cinco extratos com mesmas quantidades do produto e condições de extração, alterando apenas o solvente:
Extrato 1 - Hexano; Extrato 2 - Etanoato de etila; Extrato
3 - Água; Extrato 4 - Solução aquosa de HCl 5 %; Extrato
5 - Solução aquosa de NaOH 5 %.
Em seguida, foi feito o ensaio de inibição enzimática a
0,1 mg/mL de cada extrato, sendo obtido o gráfico abaixo:
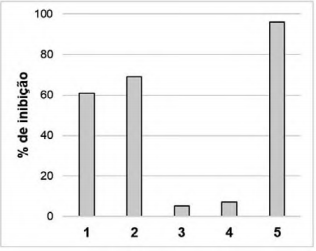
Após novos estudos, as pesquisadoras notaram que o Extrato 2 continha todas as moléculas detectadas nos outros
extratos com possível atividade inibitória. Suas estruturas
são dadas a seguir:
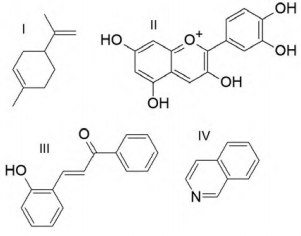
Sabendo dessas informações, a alternativa que indica o
provável composto responsável pelo efeito inibitório na
enzima é:


Gabarito comentado
Esta questão aborda o processo de extração de substâncias.
A extração
de substâncias está diretamente relacionada à solubilidade. Nesse sentido,
compostos polares são geralmente mais solúveis em solventes polares e compostos
apolares são mais solúveis em solventes apolares.
Para
determinar o provável composto responsável pelo efeito inibitório na enzima é
preciso identificar qual dos extratos apresentou maior porcentagem de inibição,
uma vez que essa substância foi extraída pelo solvente desse extrato. De acordo com o gráfico, trata-se do extrato 5,
cujo solvente é a solução aquosa de NaOH a 5%. Logo, a estrutura do composto
precisa indicar que ele seria extraído por uma base forte (NaOH). Primeiramente,
analisemos as características dos diferentes solventes utilizados para a
extração:
1 – Hexano
(C6H14): hidrocarboneto, solvente apolar;
2 – Etanoato de etila (C4H8O2): éster, solvente com características polares;
3 – Água (H2O): solvente polar;
4 – Solução aquosa de HCl (ácido clorídrico): solução ácida (HCl é um ácido forte);
5 – Solução aquosa
de NaOH 5% (hidróxido de sódio): solução básica (NaOH é uma base forte).
Com base no
exposto, analisemos os diferentes compostos:
De acordo
com as porcentagens de inibição, o composto I não é o responsável pela inibição,
pois ele é um hidrocarboneto, composto apolar, que não possui em sua molécula
algum grupo que permita a interação com a solução aquosa de NaOH, logo, ele não
seria extraído por essa solução.
Nesse
sentido, o composto II também não é o responsável pela inibição, pois ele apresenta
muitas hidroxilas (é polar) em sua molécula, grupos capazes de realizar
ligações de hidrogênio com as moléculas de água. Assim, ele seria extraído pela
molécula de H2O, mas o gráfico diz que a porcentagem de inibição
do extrato 3 é bem pequena. Esse composto possui grupos fenóis (hidroxila ligada
a um anel aromático), o que poderia tornar sua extração pela solução básica
possível. A solução básica poderia permitir a retirada do hidrogênio presente
na hidroxila do fenol, formando um sal, em que o fenol atuaria como um ácido (característica
possibilitada pela ressonância do benzeno). Entretanto, o oxigênio com carga
positiva dificulta a saída do hidrogênio, o que indica que ele não seria
extraído com facilidade pela solução de base forte.
O composto
IV também não é o responsável pela inibição, pois ele seria extraído pela
solução de HCl. Esse ácido forte é capaz de doar prótons para a o composto IV,
uma vez que ele tem o nitrogênio que recebe os prótons (é protonado a N+)
e forma um sal. Assim, através da formação desse sal solúvel na solução aquosa,
esse composto seria extraído por essa solução. Como a porcentagem de inibição
do extrato 4 é muito pequena, ele não é o responsável pela inibição.
O composto III
é o provável composto responsável pela inibição, pois ele possui em sua
estrutura um grupo fenol e uma cetona. Como grande parte da sua estrutura é
formada por carbonos e hidrogênios, ele possui uma parte apolar, que é solubilizada
no hexano, também apolar, o que indica a inibição alta do extrato 1. Ele também
é solúvel no éster, um composto com características polares e apolares solúvel
em grande parte das moléculas orgânicas (por isso extrai todas as moléculas
citadas no enunciado), o que explica a inibição alta no extrato 2. Como o
composto III possui a maior parte da cadeia com característica apolar, ele não
é muito solúvel em água (altamente polar). Devido a isso, a inibição é baixa no
extrato 3. Além disso, esse composto não possui grupos que permitam reagir com
o ácido clorídrico, o que justifica a inibição baixa no extrato 4. Por fim,
esse composto, devido ao fenol presente, pode perder o hidrogênio da hidroxila, agindo
como um ácido e formando um sal, como exemplifica a reação abaixo para um fenol:
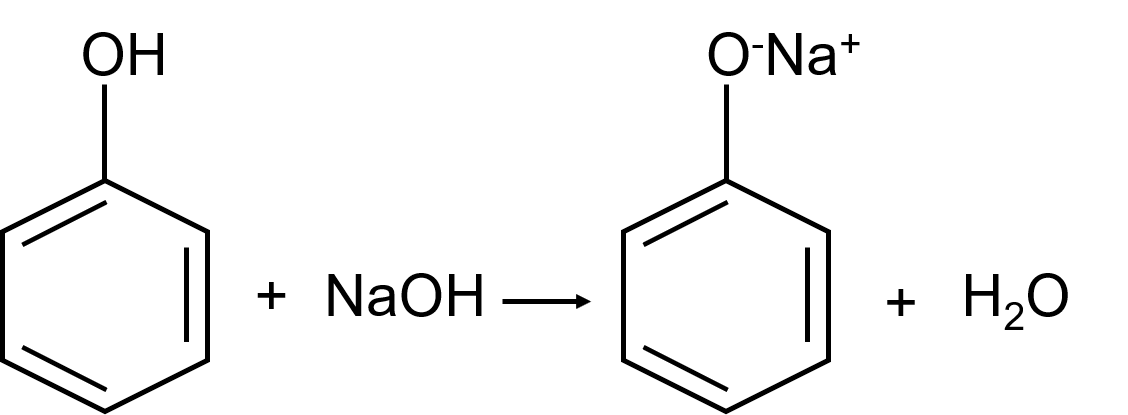
Esse sal
formado se torna solúvel na solução aquosa de NaOH, o que permite a extração, o
que explica a alta inibição do extrato 5.
Portanto, o
composto III é o provável composto responsável pela inibição.
Gabarito da Professora: Letra C.






