Selecione o item que contém a equação química balanceada que
representa adequadamente o processo Haber-Bosch.
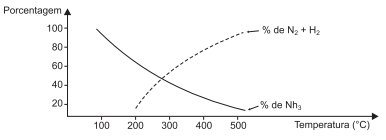
Fritz Haber, prêmio Nobel de química em 1918, ficou famoso por causa da síntese da amônia a partir do nitrogênio atmosférico, alguns meses antes da Primeira Guerra Mundial (1914-1918). A produção inicial, entre três e cinco toneladas de nitrato, aumentou rapidamente com as contribuições de Carl Bosch: em 1918 ultrapassava 300.000 toneladas anuais. O processo Haber-Bosch é uma reação entre o nitrogênio e o hidrogênio para produzir amoníaco. Esta reação é catalisada com ferro, sob as condições de 200 atmosferas de pressão e uma temperatura de 450°C.





 2 AB
2 AB


 H
H
 CH
CH H
H