Questão 9f6496da-b4
Prova:UEFS 2011
Disciplina:Química
Assunto:Equilíbrio Químico, Sistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores.
N2(g) + 3H2(g)  2NH3(g) ΔHº = − 109,5kJ
2NH3(g) ΔHº = − 109,5kJ
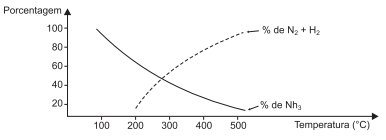
O gráfico mostra a variação do rendimento de amônia com a
variação da temperatura de acordo com o sistema em equilíbrio
químico, a 100,0atm, representado pela equação termoquímica.
Uma análise desse gráfico e do sistema em equilíbrio químico
representado pela equação termoquímica permite afirmar:

N2(g) + 3H2(g) 2NH3(g) ΔHº = − 109,5kJ
O gráfico mostra a variação do rendimento de amônia com a
variação da temperatura de acordo com o sistema em equilíbrio
químico, a 100,0atm, representado pela equação termoquímica.
Uma análise desse gráfico e do sistema em equilíbrio químico representado pela equação termoquímica permite afirmar:
A
A variação de temperatura do sistema em equilíbrio implica
variação do valor das constantes de equilíbrio Keq e Kp.
B
O aumento da temperatura do sistema em equilíbrio
químico não causa alteração no rendimento de amônia.
C
O ponto de interseção entre as curvas corresponde ao valor
da constante de equilíbrio igual à unidade.
D
A adição de catalisador ao sistema em equilíbrio provoca
alteração no rendimento de amônia.
E
A 100ºC, a percentagem de N2(g) e de H2(g) é
aproximadamente 100%.






