Questão b4637506-dd
Prova:UEFS 2010
Disciplina:Química
Assunto:Equilíbrio Químico, Sistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores.
Br2(g) + H2(g) 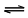 2HBr(g)
2HBr(g)
Um dado sistema em que inicialmente existem apenas
reagentes pode convergir para um estado em que há
reagentes e produtos coexistindo com concentrações
constantes ao longo do tempo. Essas concentrações não se
alteram em razão de as reações direta e inversa se
processarem com velocidades iguais, o que caracteriza um
estado de equilíbrio dinâmico.
De acordo com essas informações e considerando o sistema,
representado pela equação química, formado inicialmente pela
mistura de 1,0mol de Br2(g) com 1,0mol de H2(g), contida em
um recipiente de 10,0L, a determinada temperatura, ao atingir
o estado de equilíbrio, apresentou 0,20mol de HBr, é correto
afirmar:
Br2(g) + H2(g) 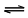 2HBr(g)
2HBr(g)
Um dado sistema em que inicialmente existem apenas reagentes pode convergir para um estado em que há reagentes e produtos coexistindo com concentrações constantes ao longo do tempo. Essas concentrações não se alteram em razão de as reações direta e inversa se processarem com velocidades iguais, o que caracteriza um estado de equilíbrio dinâmico.
De acordo com essas informações e considerando o sistema,
representado pela equação química, formado inicialmente pela
mistura de 1,0mol de Br2(g) com 1,0mol de H2(g), contida em
um recipiente de 10,0L, a determinada temperatura, ao atingir
o estado de equilíbrio, apresentou 0,20mol de HBr, é correto
afirmar:
A
A concentração de Br2 no sistema em equilíbrio é igual
a 9,0.10–2 mol.L−1
.
B
A constante de equilíbrio, Kc, é representada pela
expressão
C
O valor da constante de equilíbrio, Kc, é 16.
D
O aumento de x mol.L−1
na concentração de HBr implica
diminuição de x mol.L−1
na concentração de hidrogênio.
E
O sistema, ao atingir novo estado de equilíbrio em razão
da adição de H2(g), apresenta concentração de Br2(g)
maior que a concentração no estado anterior.






