Questão aa986677-b4
Prova:UEFS 2010
Disciplina:Química
Assunto:Substâncias e suas propriedades, Equilíbrio Químico, Sistemas Homogêneos: Equilíbrio Químico na Água: pH e pOH, Indicadores Ácido-Base, Solução Tampão., Sistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação., Interações Atômicas: Geometria Molecular, Polaridade da ligação e da Molécula, Forças Intermoleculares e Número de Oxidação., Substâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base., Soluções e Substâncias Inorgânicas
I. CaC2(s) + N2(g) 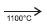 CaNCN(s) + C(s)
CaNCN(s) + C(s)
II. CaNCN(s) + 5H2O(ℓ) → CaCO3(s) + 2NH4OH(aq)
Quando carbeto de cálcio, CaC2, é aquecido em um forno
elétrico, na presença de nitrogênio atmosférico, a 1100ºC, dá
origem à cianamida de cálcio, empregada largamente como
fertilizante nitrogenado de ação lenta, pois leva alguns meses,
no solo, para se hidrolisar de acordo com a equação
química II. Como a cianamida de cálcio não é arrastada pelas
chuvas, é um fertilizante melhor do que o nitrato de amônio,
NH4NO3, e a ureia, CO(NH2)2.
Uma análise dessas informações permite afirmar:
I. CaC2(s) + N2(g) 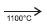 CaNCN(s) + C(s)
CaNCN(s) + C(s)
II. CaNCN(s) + 5H2O(ℓ) → CaCO3(s) + 2NH4OH(aq)
Quando carbeto de cálcio, CaC2, é aquecido em um forno elétrico, na presença de nitrogênio atmosférico, a 1100ºC, dá origem à cianamida de cálcio, empregada largamente como fertilizante nitrogenado de ação lenta, pois leva alguns meses, no solo, para se hidrolisar de acordo com a equação química II. Como a cianamida de cálcio não é arrastada pelas chuvas, é um fertilizante melhor do que o nitrato de amônio, NH4NO3, e a ureia, CO(NH2)2.
Uma análise dessas informações permite afirmar:
A
A equação química I representa uma reação de
neutralização.
B
O íon cianamida (NCN)2−
tem forma geométrica linear.
C
Os fertilizantes nitrogenados NH4NO3 e CO(NH2)2 são
insolúveis em água.
D
O pH da solução obtida após a hidrólise da cianamida
de cálcio é menor que 7.
E
A hidrólise da cianamida de cálcio, representada pela
equação química II, à temperatura ambiente, é rápida.
Estatísticas
Aulas sobre o assunto
- •
Interações Atômicas: Geometria Molecular, Polaridade da ligação e da Molécula, Forças Intermoleculares e Número de Oxidação.
Substâncias e suas propriedades
2 aulas
Substâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base.
Soluções e Substâncias Inorgânicas
3 aulas
Soluções e Substâncias Inorgânicas
4 aulas
Substâncias e suas propriedades
13 aulas






