Questão 1136fbd6-e4
Prova:UFGD 2010
Disciplina:Química
Assunto:Teoria Atômica: átomos e sua estrutura - número atômico, número de massa, isótopos, massa atômica, Transformações Químicas: elementos químicos, tabela periódica e reações químicas, Transformações Químicas
Dentro do período apresentado a seguir, a primeira energia de ionização aumenta do Sódio para o Cloro.
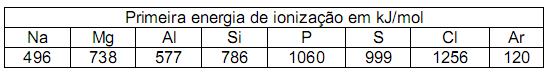
No entanto, apresenta duas exceções: o Alumínio e o Enxofre. A diminuição da energia de ionização do fósforo para o enxofre pode ser explicada pelo fato de
Dentro do período apresentado a seguir, a primeira energia de ionização aumenta do Sódio para o Cloro.

No entanto, apresenta duas exceções: o Alumínio e o Enxofre. A diminuição da energia de ionização do fósforo para o enxofre pode ser explicada pelo fato de

No entanto, apresenta duas exceções: o Alumínio e o Enxofre. A diminuição da energia de ionização do fósforo para o enxofre pode ser explicada pelo fato de
A
os elétrons no Enxofre estarem mais próximos do núcleo que os do Fósforo.
B
existir um elétron emparelhado no subnível 3p do Enxofre provocando maior repulsão.
C
o aumento do número de elétrons tornar mais fácil a sua remoção do átomo.
D
o último elétron do Enxofre possuir mais energia que o do Fósforo.
E
o átomo de Enxofre ser instável a temperatura ambiente.






