d9f28910-66
UNIFESP 2006 - Química - Sistemas Gasosos - Lei, Teoria Cinética, Equação e Mistura dos Gases. Princípio de Avogadro., Transformações Químicas
A figura representa um experimento de coleta de 0,16 g de gás oxigênio em um tubo de ensaio inicialmente preenchido com água destilada a 27 °C.
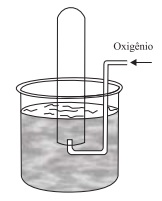
Quando o nível da água dentro do tubo de ensaio é o mesmo que o nível de fora, a pressão no interior do tubo é de 0,86 atm. Dadas a pressão de vapor (H2O) a 27 °C = 0,040 atm e R = 0,082 atm·L·K–1 ·mol –1 , o volume de gás, em mL, dentro do tubo de ensaio é igual a
A figura representa um experimento de coleta de 0,16 g de gás oxigênio em um tubo de ensaio inicialmente preenchido com água destilada a 27 °C.

Quando o nível da água dentro do tubo de ensaio é o mesmo que o nível de fora, a pressão no interior do tubo é de 0,86 atm. Dadas a pressão de vapor (H2O) a 27 °C = 0,040 atm e R = 0,082 atm·L·K–1 ·mol –1 , o volume de gás, em mL, dentro do tubo de ensaio é igual a

Quando o nível da água dentro do tubo de ensaio é o mesmo que o nível de fora, a pressão no interior do tubo é de 0,86 atm. Dadas a pressão de vapor (H2O) a 27 °C = 0,040 atm e R = 0,082 atm·L·K–1 ·mol –1 , o volume de gás, em mL, dentro do tubo de ensaio é igual a
A
30.
B
140.
C
150.
D
280.
E
300.


 Nessa reação os produtos da decomposição são CO,
Nessa reação os produtos da decomposição são CO,  e MgO (massa molar 40 g/mol). Neste gráfico são apresentados os valores da massa da amostra em função da temperatura.
e MgO (massa molar 40 g/mol). Neste gráfico são apresentados os valores da massa da amostra em função da temperatura.