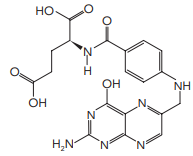
BICARBONATO DE SÓDIO PARA
COMBATER RESFRIADOS E GRIPES
Pode ajudar a manter um correto equilíbrio no
pH do sangue, o que ajuda a combater e evitar as gripes e
resfriados. Em 1924, o Dr. Volney S. Cheney, um médico
que trabalhou para o serviço de saúde pública nos Estados
Unidos, publicou o artigo “Arm & Hammer Baking Soda
Medical Use” no qual relatou os resultados de alguns
testes usando o bicarbonato de sódio, e o resultado foi
que quem fez o tratamento com esse mágico mineral não
contraiu nenhum resfriado ou gripe. O tratamento para
resfriados, usando bicarbonato de sódio, é muito fácil de
fazer, junte 1/2 colher de chá (0,03 mol) de bicarbonato
de sódio em um copo de água fria (100 mL) e beba em
seguida. Deve-se beber um copo de manhã e outro à
noite até os sintomas do resfriado desaparecerem por
completo.
Disponível em:
http://www.remedios-caseiros.com/remedios/bicarbonatode-sodio.html. Adaptada.
Acesso em: 11 de agosto de 2015.
[Dados: Kw = 1 · 10–14; Ka(H2CO3) = 4,3 · 10–7; √69 ≅ 8,3; 3/4,3 ≅ 0,69; log 8,3 ≅ 0,92]
De acordo com o texto, é pertinente inferir que o pH da
solução de bicarbonato de sódio é, aproximadamente,