Explosões são reações químicas que liberam muita energia.
A energia liberada em explosões tem como parâmetro
de medição o equivalente em tinitrotolueno (TNT) que, ao
explodir, produz 4,2 x 102J por cada 1 g.
A bomba atômica que foi lançada sobre Hiroshima (em
1945) produziu uma explosão com energia de 6,3 x 1013 J.
A quantidade, em mol, de TNT, que produziria uma energia
dessa magnitude, assumindo uma reação com 100%
de rendimento, seria:

Explosões são reações químicas que liberam muita energia. A energia liberada em explosões tem como parâmetro de medição o equivalente em tinitrotolueno (TNT) que, ao explodir, produz 4,2 x 102J por cada 1 g.
A bomba atômica que foi lançada sobre Hiroshima (em 1945) produziu uma explosão com energia de 6,3 x 1013 J. A quantidade, em mol, de TNT, que produziria uma energia dessa magnitude, assumindo uma reação com 100% de rendimento, seria:


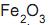 e impurezas. Ao se misturar 4,0 g de uma amostra deste minério com ácido clorídrico concentrado, obtêm- se 6,5 g de cloreto de ferro III. A porcentagem em massa de
e impurezas. Ao se misturar 4,0 g de uma amostra deste minério com ácido clorídrico concentrado, obtêm- se 6,5 g de cloreto de ferro III. A porcentagem em massa de 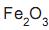 no minério é igual a
no minério é igual a