A reação de redução do cobre ocorre na etapa



A obtenção de óleos vegetais, de maneira geral, passa pelas etapas descritas no quadro.
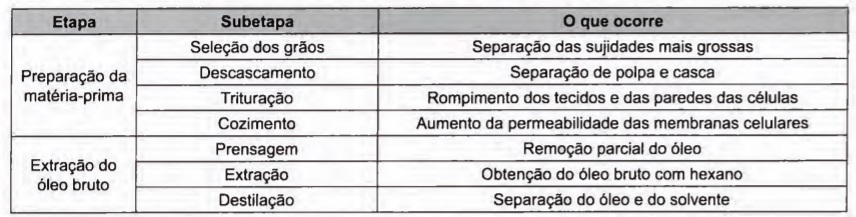
Qual das subetapas do processo é realizada em função apenas da polaridade das substâncias?
O grafeno é uma forma alotrópica do carbono constituído por uma folha planar (arranjo bidimensional) de átomos de carbono compactados e com a espessura de apenas um átomo. Sua estrutura é hexagonal, conforme a figura.

Nesse arranjo, os átomos de carbono possuem hibridação
Na Idade Média, para elaborar preparados a partir de plantas produtoras de óleos essenciais, as coletas das espécies eram realizadas ao raiar do dia. Naquela época, essa prática era fundamentada misticamente pelo efeito mágico dos raios lunares, que seria anulado pela emissão dos raios solares. Com a evolução da ciência, foi comprovado que a coleta de algumas espécies ao raiar do dia garante a obtenção de material com maiores quantidades de óleos essenciais.
A explicação científica que justifica essa prática se baseia na
Partículas microscópicas existentes na atmosfera funcionam como núcleos de condensação de vapor de água que, sob condições adequadas de temperatura e pressão, propiciam a formação das nuvens e consequentemente das chuvas. No ar atmosférico, tais partículas são formadas pela reação de ácidos (HX com a base NH3, de forma natural ou antropogênica, dando origem a sais de amônio (NH4X , de acordo com a equação química genérica:
HX (g) + NH3 (g) → NH4X (s)
FELIX, E. P.; CARDOSO, A. A. Fatores ambientais que afetam a precipitação úmida. Química Nova na Escola, n. 21, maio 2005 (adaptado).
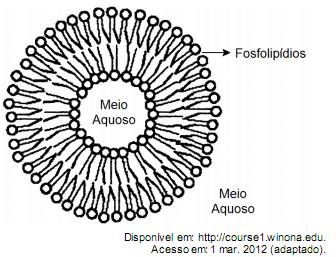
A fixação de moléculas de vapor de água pelos núcleos
de condensação ocorre por