Questão 66ac59b2-fd
Prova:INSPER 2019
Disciplina:Química
Assunto:Transformações Químicas e Energia
O fenômeno climático das monções, que ocorre na Ásia,
propicia a dispersão de poluentes que formam particulados,
como o sulfato de amônio [(NH4)2SO4]. Esse composto é formado na atmosfera pela reação da amônia (NH3) com o dióxido de enxofre (SO2), de acordo com as equações:
SO2 (g)+ 1/2O2(g) → SO3 (g)
H2O (ℓ)+SO3(g) → H2SO4 (ℓ)
2NH3 (g) + H2SO4 (ℓ) → (NH4)2SO4 (s)
Considere os valores de entalpia-padrão de formação:
SO2 (g) 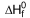 = -298 kJ/mol
= -298 kJ/mol
NH3 (g) 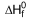 = -46 kJlmol
= -46 kJlmol
H2O (ℓ) 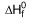 = -286 kJ/mol
= -286 kJ/mol
(NH4)2SO4 (s) 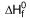 = -1179 kJ/mol
= -1179 kJ/mol
Com base nas informações apresentadas, pode-se afirmar
que a entalpia-padrão de reação de formação de 1 mol de
sulfato de amônio é
O fenômeno climático das monções, que ocorre na Ásia, propicia a dispersão de poluentes que formam particulados, como o sulfato de amônio [(NH4)2SO4]. Esse composto é formado na atmosfera pela reação da amônia (NH3) com o dióxido de enxofre (SO2), de acordo com as equações:
SO2 (g)+ 1/2O2(g) → SO3 (g)
H2O (ℓ)+SO3(g) → H2SO4 (ℓ)
2NH3 (g) + H2SO4 (ℓ) → (NH4)2SO4 (s)
Considere os valores de entalpia-padrão de formação:
SO2 (g) 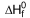 = -298 kJ/mol
= -298 kJ/mol
NH3 (g) 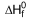 = -46 kJlmol
= -46 kJlmol
H2O (ℓ) 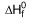 = -286 kJ/mol
= -286 kJ/mol
(NH4)2SO4 (s) 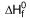 = -1179 kJ/mol
= -1179 kJ/mol
Com base nas informações apresentadas, pode-se afirmar
que a entalpia-padrão de reação de formação de 1 mol de
sulfato de amônio é

A
+503 kJ.
B
-630 kJ.
C
-503 kJ.
D
+630 kJ.
E
-1855 kJ.
Estatísticas
Aulas sobre o assunto
- •
Interações Atômicas: Ligações Iônicas, Ligações Covalentes e Ligações Metálicas. Ligas Metálicas.
Substâncias e suas propriedades
6 aulas
Interações Atômicas: Geometria Molecular, Polaridade da ligação e da Molécula, Forças Intermoleculares e Número de Oxidação.
Substâncias e suas propriedades
2 aulas
Número da Oxidação
Substâncias e suas propriedades
1 aulas
Estudo da matéria: substâncias, misturas, processos de separação.
Substâncias e suas propriedades
2 aulas
Forças Intermoleculares
Substâncias e suas propriedades
1 aulas
Transformações: Estados Físicos e Fenômenos
Substâncias e suas propriedades
1 aulas
Estrutura Atômica: números de massa, átomo neutro e íon, elemento químico e semelhanças atômicas
Transformações Químicas
2 aulas
Tabela Periódica: elementos químicos, propriedades periódicas e reações químicas
Transformações Químicas
5 aulas
Estudo dos Gases - Lei, Teoria Cinética, Equação e Mistura dos Gases. Princípio de Avogadro.
Transformações Químicas
4 aulas
Teoria Atômica: Modelo atômico de Dalton, Thomson, Rutherford, Rutherford-Bohr
Transformações Químicas
4 aulas
Substâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base.
Soluções e Substâncias Inorgânicas
3 aulas
Substâncias Inorgânicas e suas características: Ácidos, Bases, Sais e Óxidos. Reações de Neutralização.
Soluções e Substâncias Inorgânicas
1 aulas
Transformações Químicas
15 aulas
Substâncias e suas propriedades
13 aulas
Soluções e Substâncias Inorgânicas
4 aulas






