As energias de ativação das reações catalisada e não catalisada de inversão da sacarose, representadas na figura, são dadas, respectivamente, pelas diferenças (E3 – E1) e (E2 – E1).

A molécula de sacarose, em contato com a água, sofre uma
reação na qual se degrada em moléculas de glicose e frutose,
conforme o esquema acima. Essa reação, conhecida como reação de
inversão da sacarose, é catalisada em meio ácido. A sacarose desvia
o plano da luz polarizada para a direita, e uma mistura equimolar de
glicose e frutose é desviada para a esquerda, podendo o andamento
da reação ser acompanhado por intermédio de um polarímetro, que
mede o desvio da luz polarizada. A figura a seguir apresenta, de
forma esquemática, as curvas de energia potencial para as reações
catalisada e não catalisada de inversão da sacarose.

A partir dessas informações, julgue os próximos itens.

A molécula de sacarose, em contato com a água, sofre uma
reação na qual se degrada em moléculas de glicose e frutose,
conforme o esquema acima. Essa reação, conhecida como reação de
inversão da sacarose, é catalisada em meio ácido. A sacarose desvia
o plano da luz polarizada para a direita, e uma mistura equimolar de
glicose e frutose é desviada para a esquerda, podendo o andamento
da reação ser acompanhado por intermédio de um polarímetro, que
mede o desvio da luz polarizada. A figura a seguir apresenta, de
forma esquemática, as curvas de energia potencial para as reações
catalisada e não catalisada de inversão da sacarose.

A partir dessas informações, julgue os próximos itens.
Gabarito comentado
Catalisador é uma
substância química que não participa da reação química. Diminui a energia de
ativação e aumenta a velocidade da reação. O catalisador acelera a reação, mas
não altera a composição química dos reagentes e produtos envolvidos. A
quantidade de substância produzida na reação não se altera com o uso de
catalisadores. Se a reação for reversível, a reação inversa também será
acelerada, pois sua energia de ativação também terá um valor menor. O
catalisador não altera a variação de entalpia.
Gráficos com e sem catalisadores:
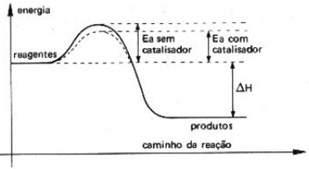
fonte: http://www.soq.com.br/conteudos/em/cineticaquimica/p6.php
A energia de
ativação da reação não catalisada representada na figura, é dado pela diferença
(E3 – E1),
enquanto que para a reação catalisada é representada pela diferença e (E2 – E1).
Item incorreto.






