Questão 2d6c4de7-b9
Prova:UNB 2023
Disciplina:Química
Assunto:Transformações Químicas e Energia
Tendo o texto precedente como referência inicial, julgue o item.
Na célula a combustível, a função do catalisador é reagir
com os íons hidrogênio, com a molécula de oxigênio e com
os elétrons recebidos do anodo para gerar energia.
Tendo o texto precedente como referência inicial, julgue o item.
Na célula a combustível, a função do catalisador é reagir com os íons hidrogênio, com a molécula de oxigênio e com os elétrons recebidos do anodo para gerar energia.
Em 1839, Sir William Grove inventou a primeira célula a
combustível. Ele sabia que, ao passar uma corrente elétrica
através da água, ela poderia ser dividida em hidrogênio e
oxigênio (um processo chamado eletrólise). Ele levantou a
hipótese de que, invertendo-se o procedimento, seria possível
produzir eletricidade e água. Ele criou uma célula a combustível
primitiva e a chamou de bateria voltaica a gás. Depois de
experimentar sua nova invenção, Grove comprovou sua hipótese.
Cinquenta anos depois, os cientistas Ludwig Mond e Charles
Langer cunharam o termo “célula a combustível” enquanto
tentavam construir um modelo prático para produzir eletricidade.
Células a combustível são excelentes para a utilização do
hidrogênio como alternativa aos combustíveis fósseis,
considerados “vilões” do aquecimento global. Elas funcionam da
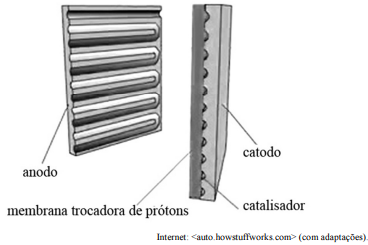
seguinte forma: o anodo, o polo negativo da célula, conduz os
elétrons liberados das moléculas de hidrogênio para um circuito
elétrico. O catodo, o polo positivo da célula, possui canais nele
gravados que distribuem o oxigênio para a superfície do
catalisador. O catodo também conduz os elétrons do circuito
elétrico para o catalisador, onde eles se unem aos íons hidrogênio
e ao oxigênio para formar água.
Em 1839, Sir William Grove inventou a primeira célula a
combustível. Ele sabia que, ao passar uma corrente elétrica
através da água, ela poderia ser dividida em hidrogênio e
oxigênio (um processo chamado eletrólise). Ele levantou a
hipótese de que, invertendo-se o procedimento, seria possível
produzir eletricidade e água. Ele criou uma célula a combustível
primitiva e a chamou de bateria voltaica a gás. Depois de
experimentar sua nova invenção, Grove comprovou sua hipótese.
Cinquenta anos depois, os cientistas Ludwig Mond e Charles
Langer cunharam o termo “célula a combustível” enquanto
tentavam construir um modelo prático para produzir eletricidade.

Células a combustível são excelentes para a utilização do
hidrogênio como alternativa aos combustíveis fósseis,
considerados “vilões” do aquecimento global. Elas funcionam da
seguinte forma: o anodo, o polo negativo da célula, conduz os
elétrons liberados das moléculas de hidrogênio para um circuito
elétrico. O catodo, o polo positivo da célula, possui canais nele
gravados que distribuem o oxigênio para a superfície do
catalisador. O catodo também conduz os elétrons do circuito
elétrico para o catalisador, onde eles se unem aos íons hidrogênio
e ao oxigênio para formar água.
C
Certo
E
Errado
Estatísticas
Aulas sobre o assunto
- •
Interações Atômicas: Ligações Iônicas, Ligações Covalentes e Ligações Metálicas. Ligas Metálicas.
Substâncias e suas propriedades
6 aulas
Interações Atômicas: Geometria Molecular, Polaridade da ligação e da Molécula, Forças Intermoleculares e Número de Oxidação.
Substâncias e suas propriedades
2 aulas
Número da Oxidação
Substâncias e suas propriedades
1 aulas
Estudo da matéria: substâncias, misturas, processos de separação.
Substâncias e suas propriedades
2 aulas
Forças Intermoleculares
Substâncias e suas propriedades
1 aulas
Transformações: Estados Físicos e Fenômenos
Substâncias e suas propriedades
1 aulas
Estrutura Atômica: números de massa, átomo neutro e íon, elemento químico e semelhanças atômicas
Transformações Químicas
2 aulas
Tabela Periódica: elementos químicos, propriedades periódicas e reações químicas
Transformações Químicas
5 aulas
Estudo dos Gases - Lei, Teoria Cinética, Equação e Mistura dos Gases. Princípio de Avogadro.
Transformações Químicas
4 aulas
Teoria Atômica: Modelo atômico de Dalton, Thomson, Rutherford, Rutherford-Bohr
Transformações Químicas
4 aulas
Substâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base.
Soluções e Substâncias Inorgânicas
3 aulas
Substâncias Inorgânicas e suas características: Ácidos, Bases, Sais e Óxidos. Reações de Neutralização.
Soluções e Substâncias Inorgânicas
1 aulas
Transformações Químicas
15 aulas
Substâncias e suas propriedades
13 aulas
Soluções e Substâncias Inorgânicas
4 aulas






