A atividade física intensa e prolongada causa a transpiração do corpo e, assim, a perda de sais minerais, principalmente
sais de sódio, importantes para o equilíbrio orgânico, que tecnicamente chamam-se hidro-eletrolíticos. Isso ocorre porque
minerais como sódio, potássio, magnésio e cálcio são importantes para a maioria das funções de contração muscular do
nosso corpo. Esses minerais, perdidos pelo suor − cuja densidade média é 1,004 g/L − durante a transpiração, podem ser
repostos pela ingestão de bebidas isotônicas, melhorando o desempenho esportivo.
Considerando as informações do texto, têm-se as seguintes afirmativas:
I - O suor é uma mistura heterogênea do tipo suspensão.
II - A densidade do suor é a razão entre seu volume e sua massa e representa uma propriedade química.
III - O suor sobre a pele desaparece quando o atleta pára de jogar, porque retira energia térmica do corpo para transformar
seu estado físico de líquido para gasoso.
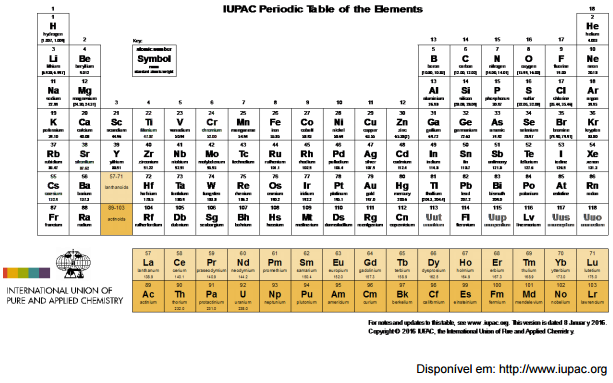
IV - Os íons sódio e potássio, contidos no suor, são metais alcalinos e pertencem ao primeiro grupo da tabela periódica.
V - Os íons sódio, potássio e magnésio, liberados durante a transpiração, possuem cargas iguais a +1, +1 e +2,
respectivamente.
Assinale a alternativa que reúne somente afirmativas corretas.