Fe2+(aq) + HCO-3 + O2(aq) → Fe2O3(s) + CO2(g) + H2O(l)
A presença de sais de ferro, a exemplo de bicarbonato de
ferro (II), Fe(HCO3)2(aq), na água de abastecimento, deixa
manchas de cor marrom quando a água goteja sobre a
superfície de azulejos, pisos e vasos sanitários, em razão da
formação de depósitos de óxido de ferro (III), Fe2O3(s).
Após análise dessas informações e do balanceamento da
equação química com coeficientes estequiométricos inteiros,
é correto afirmar:
Fe2+(aq) + HCO-3 + O2(aq) → Fe2O3(s) + CO2(g) + H2O(l)
A presença de sais de ferro, a exemplo de bicarbonato de ferro (II), Fe(HCO3)2(aq), na água de abastecimento, deixa manchas de cor marrom quando a água goteja sobre a superfície de azulejos, pisos e vasos sanitários, em razão da formação de depósitos de óxido de ferro (III), Fe2O3(s).
Após análise dessas informações e do balanceamento da
equação química com coeficientes estequiométricos inteiros,
é correto afirmar:
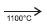 CaNCN(s) + C(s)
CaNCN(s) + C(s)
 Na
Na