Questõesde FATEC sobre Equilíbrio Químico
A reação de esterificação é uma reação reversível; portanto,
em um sistema fechado, atinge-se o equilíbrio químico.
A produção da essência de maçã-verde pode ser
favorecida pelo deslocamento desse equilíbrio por meio

Certa solução aquosa de bicarbonato de sódio,
NaHCO3
, apresenta pH = 8,3 a 25º C. Tal solução é
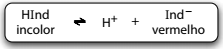
A fenolftaleína atua como um indicador ácido-base por
ser um ácido fraco, que em solução alcóolica, apresenta a
cor das moléculas não-dissociadas, HInd, diferente da cor
dos respectivos íons, Ind–.
A leitura da mensagem no experimento descrito é possível
porque a presença de íons OH– na solução de fenolftaleína
promove deslocamento do equilíbrio para a
A fenolftaleína atua como um indicador ácido-base por ser um ácido fraco, que em solução alcóolica, apresenta a cor das moléculas não-dissociadas, HInd, diferente da cor dos respectivos íons, Ind–.

A leitura da mensagem no experimento descrito é possível
porque a presença de íons OH– na solução de fenolftaleína
promove deslocamento do equilíbrio para a
Experiência – Escrever uma mensagem secreta no laboratório
Materiais e Reagentes Necessários
✓ Folha de papel
✓ Pincel fino
✓ Difusor
✓ Solução de fenolftaleína
✓ Solução de hidróxido de sódio 0,1 mol/L ou solução saturada de hidróxido de cálcio
Procedimento Experimental
Utilizando uma solução incolor de fenolftaleína, escreva com um pincel fino uma mensagem numa folha de papel.
A mensagem permanecerá invisível.
Para revelar essa mensagem, borrife a folha de papel com uma solução de hidróxido de sódio ou de cálcio, com o auxílio de um difusor.
A mensagem aparecerá magicamente com a cor vermelha.
Explicação
fenolftaleína é um indicador que fica vermelho na presença de soluções básicas, nesse caso, uma solução de hidróxido de sódio ou de cálcio.
Para obtermos 100 mL de uma solução aquosa saturada
de hidróxido de cálcio, Ca(OH)2, para o experimento,
devemos levar em consideração a solubilidade desse
composto.
Sabendo que o produto de solubilidade do hidróxido de
cálcio é 5,5 x 10-6, a 25 °C, a solubilidade dessa base em
mol/L é, aproximadamente,
Dados:
Ca(OH)2(s) ⇌ Ca2+(aq) + 2OH–(aq)
Kps = [Ca2+] . [OH–]
2
Para obtermos 100 mL de uma solução aquosa saturada de hidróxido de cálcio, Ca(OH)2, para o experimento, devemos levar em consideração a solubilidade desse composto.
Sabendo que o produto de solubilidade do hidróxido de cálcio é 5,5 x 10-6, a 25 °C, a solubilidade dessa base em mol/L é, aproximadamente,
Dados:
Ca(OH)2(s) ⇌ Ca2+(aq) + 2OH–(aq)
Kps = [Ca2+] . [OH–]
2
Experiência – Escrever uma mensagem secreta no laboratório
Materiais e Reagentes Necessários
✓ Folha de papel
✓ Pincel fino
✓ Difusor
✓ Solução de fenolftaleína
✓ Solução de hidróxido de sódio 0,1 mol/L ou solução saturada de hidróxido de cálcio
Procedimento Experimental
Utilizando uma solução incolor de fenolftaleína, escreva com um pincel fino uma mensagem numa folha de papel.
A mensagem permanecerá invisível.
Para revelar essa mensagem, borrife a folha de papel com uma solução de hidróxido de sódio ou de cálcio, com o auxílio de um difusor.
A mensagem aparecerá magicamente com a cor vermelha.
Explicação
fenolftaleína é um indicador que fica vermelho na presença de soluções básicas, nesse caso, uma solução de hidróxido de sódio ou de cálcio.
Na indústria têxtil, é uma prática comum aplicar goma aos tecidos no início da produção, para torná-los mais resistentes.
Esse produto, entretanto, precisa ser removido posteriormente, no processo de desengomagem. Nesse processo, os
produtos têxteis são mergulhados em um banho aquoso com uma enzima do grupo das amilases.
Os gráficos nas figuras 1 e 2 representam a eficiência da atividade dessa enzima em diferentes valores de temperatura
e pH.

Com base nas informações apresentadas, está correto afirmar que, para se obter a máxima eficiência da ação da enzima no
processo industrial citado no texto, seria necessário manter o banho aquoso de desengomagem a
Na indústria têxtil, é uma prática comum aplicar goma aos tecidos no início da produção, para torná-los mais resistentes. Esse produto, entretanto, precisa ser removido posteriormente, no processo de desengomagem. Nesse processo, os produtos têxteis são mergulhados em um banho aquoso com uma enzima do grupo das amilases.
Os gráficos nas figuras 1 e 2 representam a eficiência da atividade dessa enzima em diferentes valores de temperatura e pH.

Com base nas informações apresentadas, está correto afirmar que, para se obter a máxima eficiência da ação da enzima no
processo industrial citado no texto, seria necessário manter o banho aquoso de desengomagem a
A escala de pH que varia de 0 a 14 é válida apenas para
sistemas aquosos a 25 °C. Variando-se a temperatura, a
escala de pH também varia.
O quadro fornece valores de Kw e de pH da água pura em
diferentes temperaturas
Temperatura (°C) Kw pH 0 1,14 × 10–15 7,47 10 2,95 × 10–15 7,27 20 1,00 × 10–14 7,00 30 1,47 × 10–14 6,83 50 5,30 × 10–14 6,27
Analisando-se os dados, pode-se afirmar, corretamente,
que a
Uma das substâncias responsáveis pelo cheiro desagradável que as pessoas sentem, ao passarem nas proximidades de rios e de
córregos poluídos por esgoto, é o sulfeto de hidrogênio, H2S (g). Esse mau cheiro se intensifica principalmente em dias quentes, pois
o aumento de temperatura diminui a solubilidade desse gás em água.
Quando borbulhado em água, o H2S comporta-se como ácido fraco, estabelecendo-se os equilíbrios simultâneos representados pelas
equações a seguir:

Dentre os procedimentos a seguir, o único que provoca um aumento do escape de sulfeto de hidrogênio de uma solução aquosa para
o ar é
Quando borbulhado em água, o H2S comporta-se como ácido fraco, estabelecendo-se os equilíbrios simultâneos representados pelas equações a seguir:

Dentre os procedimentos a seguir, o único que provoca um aumento do escape de sulfeto de hidrogênio de uma solução aquosa para o ar é
A cor das flores de diversas plantas ocorre devido à presença de substâncias, como as antocianinas, que
atuam como indicadores ácido-base. Assim, conforme o pH do solo, a cor das flores pode variar. É o caso das
hortênsias, que apresentam cor azul em solos ácidos e rosa em solos alcalinos.
Caso uma pessoa queira cultivar hortênsias de cor rosa, em um jardim cujo solo seja ácido, ela deverá corrigir
o pH e, para isso, poderá misturar à terra, em quantidade adequada,
A cor das flores de diversas plantas ocorre devido à presença de substâncias, como as antocianinas, que atuam como indicadores ácido-base. Assim, conforme o pH do solo, a cor das flores pode variar. É o caso das hortênsias, que apresentam cor azul em solos ácidos e rosa em solos alcalinos.
Caso uma pessoa queira cultivar hortênsias de cor rosa, em um jardim cujo solo seja ácido, ela deverá corrigir o pH e, para isso, poderá misturar à terra, em quantidade adequada,
O hidróxido de sódio, NaOH (soda cáustica), é bastante solúvel em água e utilizado para a remoção de resíduos de matéria orgânica na limpeza dos equipamentos usados na fabricação de alimentos. Uma empresa alimentícia usou uma solução de hidróxido de sódio (soda cáustica) a 2,5% (m/v) para a limpeza de seus equipamentos.
Essa solução apresenta pH elevado, aproximadamente 13, a 25°C, e que pode representar risco de queimadura ou sensação de forte ardência na boca, caso venha a ser ingerida.
Considerando o pH, a 25°C, da solução mencionada no texto, temos meio.
Dado: Produto iônico da água,
Kw=1,0• 10–14 , a 25°C.
Essa solução apresenta pH elevado, aproximadamente 13, a 25°C, e que pode representar risco de queimadura ou sensação de forte ardência na boca, caso venha a ser ingerida.
Considerando o pH, a 25°C, da solução mencionada no texto, temos meio.
Dado: Produto iônico da água,
Kw=1,0• 10–14 , a 25°C.
O hidróxido de sódio, NaOH (soda cáustica), é bastante solúvel em água e utilizado para a remoção de resíduos de matéria orgânica na limpeza dos equipamentos usados na fabricação de alimentos.
Uma empresa alimentícia usou uma solução de hidróxido de sódio (soda cáustica) a 2,5% (m/v) para a limpeza de seus equipamentos.
Essa solução apresenta pH elevado, aproximadamente 13, a 25°C, e que pode representar risco de queimadura ou sensação de forte ardência na boca, caso venha a ser ingerida.
A solução de NaOH, descrita no texto, apresenta concentração em mol/L, aproximadamente, de.
Uma empresa alimentícia usou uma solução de hidróxido de sódio (soda cáustica) a 2,5% (m/v) para a limpeza de seus equipamentos.
Essa solução apresenta pH elevado, aproximadamente 13, a 25°C, e que pode representar risco de queimadura ou sensação de forte ardência na boca, caso venha a ser ingerida.
A solução de NaOH, descrita no texto, apresenta concentração em mol/L, aproximadamente, de.
Considere a reação de formação da amônia N2 (g) + 3H2 (g) ⇌ 2NH3 (g) e o gráfico, que mostra a influência conjunta da pressão e da temperatura no seu rendimento.
A análise do gráfico permite concluir, corretamente, que:
A análise do gráfico permite concluir, corretamente, que:
