Muitos laboratórios armazenam em seus
estoques soluções concentradas de reagentes. Um
técnico responsável dispõe, em seu laboratório, de
uma solução de etanol (álcool absoluto) a 16,3 mol/L.
O volume de água, em litros, que deve ser adicionado
a 400 mL de solução de etanol a 16,3 mol/L (álcool
absoluto) para produzir etanol hidratado a 70 % v/v é,
aproximadamente:
(Dado: detanol = 0,8 g/mL)
Muitos laboratórios armazenam em seus estoques soluções concentradas de reagentes. Um técnico responsável dispõe, em seu laboratório, de uma solução de etanol (álcool absoluto) a 16,3 mol/L. O volume de água, em litros, que deve ser adicionado a 400 mL de solução de etanol a 16,3 mol/L (álcool absoluto) para produzir etanol hidratado a 70 % v/v é, aproximadamente:
(Dado: detanol = 0,8 g/mL)
Gabarito comentado
Esta questão
relaciona conceitos importantes para o preparo de soluções.
É desejado
preparar uma solução final de etanol hidratado com concentração igual a 70 %v/v,
a partir de uma solução inicial de etanol com concentração de 16,3 mol/L com
volume igual a 400 mL. Primeiramente é preciso organizar os dados para resolver
a questão:
Concentração
molar do etanol (MEtanol) = 16,3 mol/L;
Volume da solução de etanol (VSol. Etanol) = 400 mL = 0,4 L;
Concentração do etanol hidratado (CSol. Etanol hidratado) = 70 % v/v;
Densidade do etanol (dEtanol) = 0,8 g/ml;
Massas
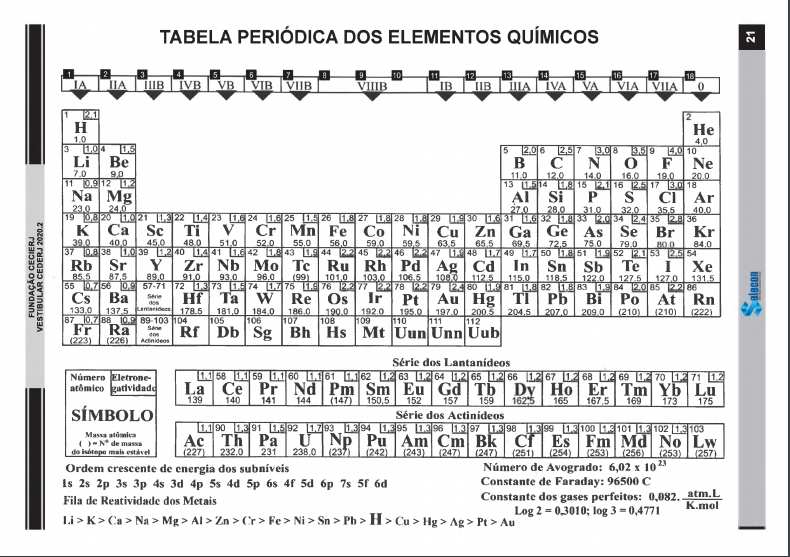
molares (fornecidas pela tabela periódica, em g/mol): C = 12; H = 1; O = 16.
1) Para
calcular o volume de água que deve ser adicionado para a obtenção da solução de
etanol com concentração 70 %v/v é preciso calcular o número de mols de etanol
contido na solução inicial, a partir da concentração molar e do volume (em litros):
nEtanol
= MEtanol × VSol. Etanol = 16,3
× 0,4 = 6,52 mol
2) Com o
número de mols é possível saber a massa de etanol na solução inicial, que será
a mesma da solução final, uma vez que para a obtenção da solução de etanol
hidratado apenas água será adicionada (diluição). A massa pode ser determinada
a partir da massa molar do etanol.
Esse composto é um álcool e possui dois carbonos (prefixo et), uma hidroxila (grupo que caracteriza a função álcool quando ligada a um carbono saturado) e seis hidrogênios (pois o carbono faz 4 ligações). Sua fórmula molecular é, dessa forma, C2H6O. Sua massa molar (MM) pode ser obtida a partir das massas molares dos elementos presentes nesse composto:
MMEtanol
= 2 × MMC + 6 × MMH
+ MMO = 2 × 12 + 6 × 1 + 16 = 46 g/mol
Com a massa molar
podemos calcular a massa de etanol presente nas soluções por regra de três,
considerando o número de mols calculado:
1 mol de Etanol possui 46 g
6,52 mol ------- m
mEtanol
= 46 × 6,52 = 299,92 g
3) A
densidade do etanol indica quantos gramas estão presentes na solução de etanol
inicial, assim, é possível saber o volume de etanol puro nessa solução por
regra de três, considerando a massa calculada acima:
0,8 g de Etanol presente em 1 mL
299,92 g ------------- VEtanol puro
VEtanol
puro = 299,92/0,8 = 374,9 mL
4) Com o
volume de etanol puro é possível saber o volume da solução de etanol hidratado.
A concentração em % volume/volume possui a seguinte expressão:
C = (Vsoluto/Vsolução) × 100
Assim,
tem-se que:
C = (VEtanol
puro/VSol. Etanol hidratado) × 100
Substituindo
os valores:
70/100 = 374,9/VSol. Etanol hidratado
VSol. Etanol hidratado = 374,9/0,7
VSol. Etanol
hidratado = 535,6 mL
5) Por fim,
com o volume total da solução de etanol hidratado, basta diminuir o valor do
volume da solução de etanol inicial para saber o volume de água adicionado:
Vágua = VSol. Etanol hidratado – VSol. Etanol
Vágua =
535,6 – 400 = 135,6 mL = (135,6/1000) L = 0,135 L
Gabarito da Professora: Letra A.






