Questão 095fa806-dd
Prova:UEM 2011, UEM 2011
Disciplina:Química
Assunto:Soluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais., Soluções e Substâncias Inorgânicas
A concentração da solução de NH4NO3
preparada é de, aproximadamente, 0,020
mol/L.
A concentração da solução de NH4NO3
preparada é de, aproximadamente, 0,020
mol/L.
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO
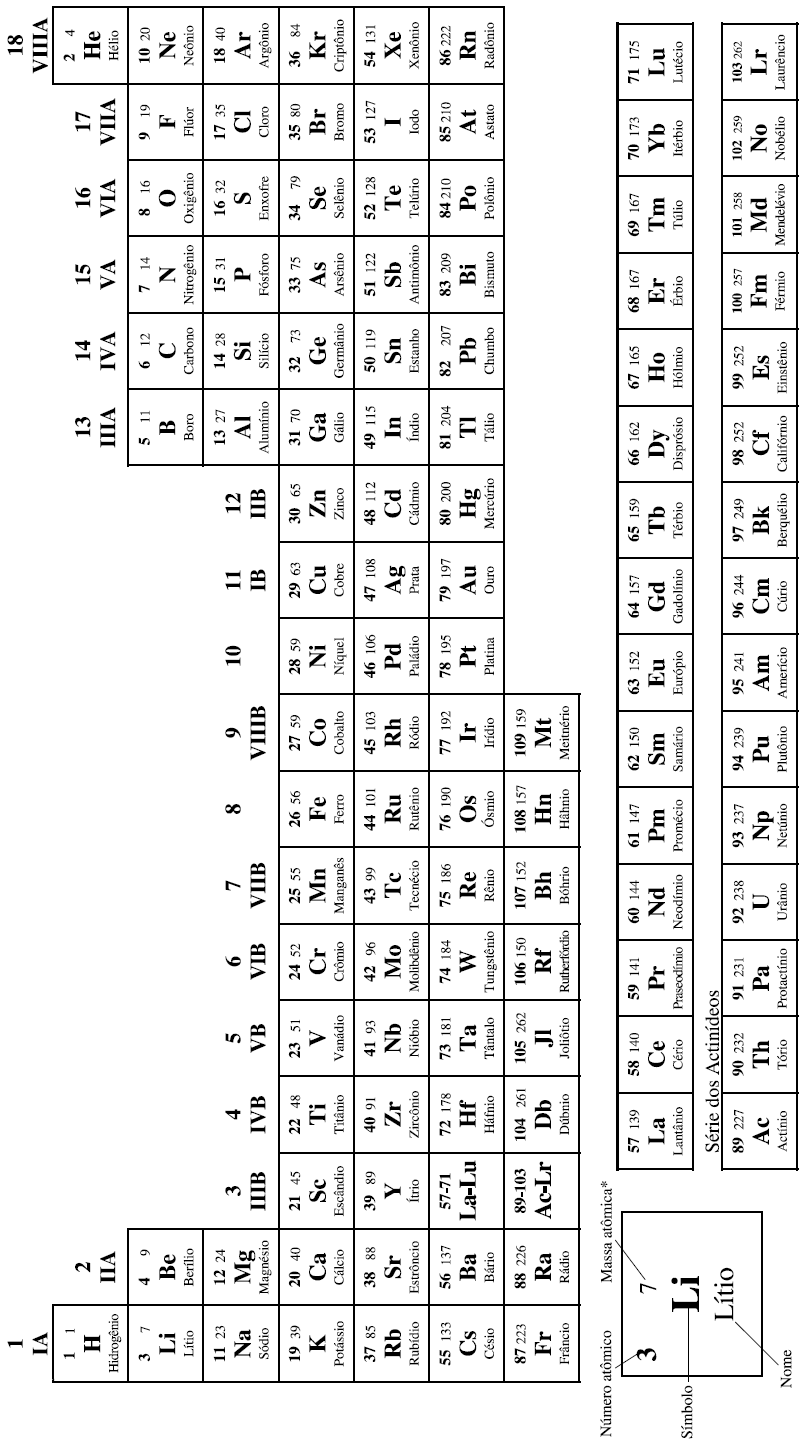
*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADAS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE PROCESSO E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Ao preparar uma solução de Ca(NO3)2 (nitrato de
cálcio) em laboratório, um aluno, inadvertidamente,
pesou 1,64 g de NH4NO3 (nitrato de amônio) por
engano e o dissolveu em água destilada,
preparando 1,0 L de solução. Considerando a
densidade da água igual a 1,0 g/mL a 25 °C, e
dadas as massas molares dos sais,
Ca(NO3)2 = 164 g/mol
NH4NO3 = 80 g/mol, assinale a alternativa correta.
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADAS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE PROCESSO E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADAS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE PROCESSO E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Ao preparar uma solução de Ca(NO3)2 (nitrato de cálcio) em laboratório, um aluno, inadvertidamente, pesou 1,64 g de NH4NO3 (nitrato de amônio) por engano e o dissolveu em água destilada, preparando 1,0 L de solução. Considerando a densidade da água igual a 1,0 g/mL a 25 °C, e dadas as massas molares dos sais,
Ca(NO3)2 = 164 g/mol
NH4NO3 = 80 g/mol, assinale a alternativa correta.
C
Certo
E
Errado






