719f171b-56
UFG 2010 - Química - Química Orgânica, Tipos de Reações Orgânicas: Substituição, Adição e Eliminação., Tipos de Reagentes e Mecanismos das Reações Orgânicas., Tipos de Reações Orgânicas: Oxidação, Redução e Polimerização.
Uma das etapas envolvidas no ciclo do ácido cítrico é a transformação do isocitrato, conforme o esquema a seguir.

A enzima envolvida nessa reação realiza um processo de
Uma das etapas envolvidas no ciclo do ácido cítrico é a transformação do isocitrato, conforme o esquema a seguir.

A enzima envolvida nessa reação realiza um processo de

A enzima envolvida nessa reação realiza um processo de
A
descarboxilação
B
oxidação
C
redução
D
neutralização
E
isomerização









 em nanômetros (nm), é igual a:
em nanômetros (nm), é igual a: 
 do fumarato é maior que o
do fumarato é maior que o  do maleato.
do maleato.







 , possui diversos isômeros de cadeia, os quais apresentam propriedades físicas diferentes. Dos isômeros a seguir, o que tem o menor ponto de ebulição é o seguinte:
, possui diversos isômeros de cadeia, os quais apresentam propriedades físicas diferentes. Dos isômeros a seguir, o que tem o menor ponto de ebulição é o seguinte:




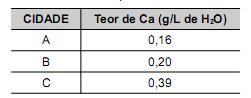
 por exemplo, é um composto utilizado para corrigir a concentração de soluções alcalinas por meio da técnica de titulometria. Uma alíquota de 5,0 mL de uma solução de H2C2O4 0,100 mol/L foi titulada com uma solução de NaOH 0,100 mol/L, utilizando-se a fenolftaleí na como indicador. De acordo com a equação química (não balanceada) apresentada a seguir
por exemplo, é um composto utilizado para corrigir a concentração de soluções alcalinas por meio da técnica de titulometria. Uma alíquota de 5,0 mL de uma solução de H2C2O4 0,100 mol/L foi titulada com uma solução de NaOH 0,100 mol/L, utilizando-se a fenolftaleí na como indicador. De acordo com a equação química (não balanceada) apresentada a seguir