Questõessobre Transformações Químicas e Energia
Considere o gráfico que representa genericamente uma
transformação exotérmica.

Energia de ativação, variação de entalpia da
transformação e complexo ativado podem ser,
respectivamente, associados aos números

No final da década de 1930, Hahn e Strassmann
estudaram a fissão nuclear do urânio, elemento que
possui número atômico igual a 92 e cujo isótopo 235
é capaz de sofrer fissão se bombardeado por um
nêutron acelerado. Nesse processo, formam-se dois
núcleos menores, são liberados nêutrons e grande
quantidade de energia. O exemplo que representa
corretamente a fissão do urânio é





No fragmento a seguir, o autor explora conceitos químicos na
forma de poesia:

Sobre os conceitos mencionados, foram feitas as seguintes
afirmações:
I. A equação química mostrada na linha 2 pode ser associada à
liberação de energia, pois corresponde à reação de
fotossíntese com consumo de gás carbônico.
II. A equação química apresentada na linha 6 representa uma
reação na qual o número de oxidação das espécies é alterado,
sendo associada a corrosão.
III. O modelo incompleto referido na linha 7 refere-se ao
proposto por Thomson, que identificava a presença de
partículas com carga negativa dentro de uma esfera.
Está correto o que se afirma no(s) item(ns):
No fragmento a seguir, o autor explora conceitos químicos na forma de poesia:

Sobre os conceitos mencionados, foram feitas as seguintes afirmações:
I. A equação química mostrada na linha 2 pode ser associada à liberação de energia, pois corresponde à reação de fotossíntese com consumo de gás carbônico.
II. A equação química apresentada na linha 6 representa uma reação na qual o número de oxidação das espécies é alterado, sendo associada a corrosão.
III. O modelo incompleto referido na linha 7 refere-se ao proposto por Thomson, que identificava a presença de partículas com carga negativa dentro de uma esfera.
Está correto o que se afirma no(s) item(ns):
Os tanques de armazenamento de gasolina podem,
com o tempo, sofrer processos oxidativos, resultando na
contaminação do combustível e do solo à sua volta. Uma
forma de evitar tais problemas econômicos e ambientais é
utilizar preferencialmente metais de sacrifício, protegendo
os tanques de armazenamento.
Suponha que seja necessário usar um metal de
sacrifício em um tanque de aço (liga de ferro-carbono).
Considere as semirreações de redução e seus respectivos
potenciais padrão.

Dos metais citados, o que garantirá proteção ao tanque
de aço é o

Com a descoberta de emissões de energia do
rádio-226, por Marie Curie e Pierre Curie, o fenômeno
foi denominado radiação α (alfa) ou emissão α.
Posteriormente, verificou-se que a emissão α na
verdade são partículas correspondentes a núcleos
de hélio formados por dois prótons e dois nêutrons.
Assim, no decaimento α, um núcleo instável emite
partículas α, tornando-se um núcleo mais estável
(núcleo filho).
Se um núcleo de rádio-226 emitir duas partículas α, o
número de massa do núcleo filho será
Um cidadão que se mudou de Brasília para Recife,
após algum tempo, percebeu que partes de seu carro
estavam enferrujando muito rapidamente. Perguntou para
seu filho, estudante do ensino médio, a explicação para o
fenômeno. O filho pesquisou na internet e descobriu que,
por causa da maresia, gotículas de água do mar atingem
os objetos de aço (liga de ferro e carbono) e intensificam
sua corrosão. Com base nessa informação, o estudante
explicou corretamente ao pai o efeito do cloreto de sódio
na corrosão.
A explicação correta de a maresia acelerar a corrosão do
aço é porque
O espintariscópio é um
aparelho quase fora de uso, munido de uma tela
de sulfeto de zinco utilizado para observar as
cintilações produzidas pelo impacto de
partículas ionizantes na tela. Sobre as
partículas ionizantes assinale a alternativa
Correta:

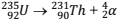

A tradição de produzir
joias e semi joias em Juazeiro do Norte vem
desde os tempos do Padre Cícero. Como a
cidade recebia muitos visitantes para casar e
não tinham alianças, surgiam daí as primeiras
oficinas de joias. A galvanoplastia utiliza a
eletrolise em meio aquoso para cobrir uma
determinada peça metálica com outro metal. Na
prateação (Ag
+
) de uma aliança, fez-se passar
pelas células uma corrente de 3,72 ampères
durante 20 minutos. Qual a massa de prata, depositada na superfície da aliança. Dados Ag =
108

As pilhas recarregáveis, bastante utilizadas atualmente, são formadas por sistemas queatuam como uma célula galvânica, enquanto estão sendo descarregadas, e como célulaeletrolítica, quando estão sendo recarregadas.
Uma pilha é formada pelos elementos níquel e cádmio e seu carregador deve forneceruma diferença de potencial mínima para promover a recarga. Quanto maior a diferença depotencial gerada pelo carregador, maior será o seu custo. Considere os valores de potencialpadrão de redução dessas espécies:
Ni2+ (aq) + 2 e− ⇌ Ni (s) E° = −0,230 V
Cd2+ (aq) + 2 e− ⇌ Cd (s) E° = −0,402 V
Teoricamente, para que um carregador seja ao mesmo tempo eficiente e tenha o menor preço,
a diferença de potencial mínima, em volt, que ele deve superar é de
As pilhas recarregáveis, bastante utilizadas atualmente, são formadas por sistemas queatuam como uma célula galvânica, enquanto estão sendo descarregadas, e como célulaeletrolítica, quando estão sendo recarregadas.
Uma pilha é formada pelos elementos níquel e cádmio e seu carregador deve forneceruma diferença de potencial mínima para promover a recarga. Quanto maior a diferença depotencial gerada pelo carregador, maior será o seu custo. Considere os valores de potencialpadrão de redução dessas espécies:
Ni2+ (aq) + 2 e− ⇌ Ni (s) E° = −0,230 V
Cd2+ (aq) + 2 e− ⇌ Cd (s) E° = −0,402 V
Teoricamente, para que um carregador seja ao mesmo tempo eficiente e tenha o menor preço,
a diferença de potencial mínima, em volt, que ele deve superar é de
Os objetos de prata tendem a escurecer com o tempo, em contato com compostos de
enxofre, por causa da formação de uma película superficial de sulfeto de prata (Ag2S), que é
escuro. Um método muito simples para restaurar a superfície original desses objetos é
mergulhá-los em uma solução diluída aquecida de hidróxido de sódio (NaOH), contida em uma
panela comum de alumínio. A equação química que ilustra esse processo é:
3 Ag2S (s) + 2 Al (s) + 8 NaOH (aq) → 6 Ag (s) + 3 Na2S (aq) + 2 NaAlO2 (aq) + 4 H2O (l)
A restauração do objeto de prata ocorre por causa do(a)
Os objetos de prata tendem a escurecer com o tempo, em contato com compostos de enxofre, por causa da formação de uma película superficial de sulfeto de prata (Ag2S), que é escuro. Um método muito simples para restaurar a superfície original desses objetos é mergulhá-los em uma solução diluída aquecida de hidróxido de sódio (NaOH), contida em uma panela comum de alumínio. A equação química que ilustra esse processo é:
3 Ag2S (s) + 2 Al (s) + 8 NaOH (aq) → 6 Ag (s) + 3 Na2S (aq) + 2 NaAlO2 (aq) + 4 H2O (l)
A restauração do objeto de prata ocorre por causa do(a)
Analise as equações termoquímicas.

A partir dessas equações, pode-se prever que o ∆H da reação de decomposição do calcário que produz cal viva (cal
virgem) e dióxido de carbono seja igual a

Analise as reações.
Reação 1 – Obtenção de água sanitária
Cℓ2
(g) + 2NaOH (aq) → NaCℓ O (aq) + NaCℓ (aq) + H2O (ℓ)
Reação 2 – Reação de carga de uma bateria chumbo/ácido
2PbSO4
(s) + 2H2O (ℓ) → Pb (s) + PbO2
(s) + 2H2SO4
(aq)
Reação 3 – Combustão de magnésio metálico
Mg (s) + 1/2 O2
(g) → MgO (s)
Reação 4 – Obtenção de cal
CaCO3
(s) → CaO (s) + CO2
(g)
São exemplos de oxirredução, que apresentam um reagente atuando simultaneamente como oxidante e redutor, as
reações
Analise as reações.
Reação 1 – Obtenção de água sanitária
Cℓ2 (g) + 2NaOH (aq) → NaCℓ O (aq) + NaCℓ (aq) + H2O (ℓ)
Reação 2 – Reação de carga de uma bateria chumbo/ácido
2PbSO4 (s) + 2H2O (ℓ) → Pb (s) + PbO2 (s) + 2H2SO4 (aq)
Reação 3 – Combustão de magnésio metálico
Mg (s) + 1/2 O2 (g) → MgO (s)
Reação 4 – Obtenção de cal
CaCO3 (s) → CaO (s) + CO2 (g)
São exemplos de oxirredução, que apresentam um reagente atuando simultaneamente como oxidante e redutor, as
reações
Embora a energia nuclear possa ser utilizada
para fins pacíficos, recentes conflitos geopolíticos
têm trazido preocupações em várias partes do
planeta e estimulado discussões visando o combate
ao uso de armas de destruição em massa. Além do
potencial destrutivo da bomba atômica, uma grande
preocupação associada ao emprego desse artefato
bélico é a poeira radioativa deixada após a bomba
ser detonada.
Qual é o processo envolvido na detonação dessa bomba?
No Museu do Louvre, estão exibidos objetos metálicos
usados por sociedades antigas. No passado, alguns
desses metais eram encontrados praticamente em seu
estado puro. Com o advento da metalurgia, puderam
ser obtidos a partir de minerais submetidos a reações
químicas.
Em relação aos processos de obtenção de metais a partir de minerais, e com base nos conhecimentos sobre
reações de oxidorredução, considere as afirmativas a
seguir.
I. Alo
(s) pode ser obtido a partir de bauxita
(Al2O3.H2O ) por meio de um método eletrolítico,
o qual é baseado num processo não espontâneo
onde Al3+ é reduzido a Alo
(s).
II. Cuo
(s) pode ser obtido a partir da queima de sulfeto de cobre, conforme reação Cu2S(s) + O2(g) →
2Cu(s) + SO2(g), onde o número de oxidação do
cobre muda de (1+) para (0).
III. Feo
(s) pode ser obtido a partir de reações de redução de óxidos de ferro conforme transformações
químicas: Fe2O3(s) → FeO2(s) → Feo
(s).
IV. Mno
(s) pode ser obtido a partir da reação MnO2(s)+
C(s) → Mn(s) + CO2(g) em que o átomo de oxigênio em MnO2(s) é o redutor e o carbono (C) é o
oxidante.
Assinale a alternativa correta.
Obras de arte expostas em museus podem conter metais tóxicos em sua composição, como chumbo, cádmio ou mercúrio e/ou seus óxidos. Um incêndio em um
museu no qual obras de arte contendo mercúrio são incineradas pode gerar dimetilmercúrio ((CH3)2Hg), uma
neurotoxina altamente letal mesmo em baixas concentrações (0,030 mg/cm3). Se inalado, os sintomas costumam aparecer semanas após a exposição inicial, o que
torna ineficaz qualquer tipo de tratamento. As equações químicas 1 e 2 são exemplos de reações químicas
de formação do composto dimetilmercúrio.
Equação 1:
3C2H6(g) + 2HgO(s) + 5/2
O2(g) → 2(CH3)2Hg(g) + 2CO2(g) +
3H2O(g)
Equação 2:
3C2H5OH(g) + HgO(s) + 5O2(g) → (CH3)2Hg(g) + 4CO2(g) +
6H2O(g)

Com base no texto, nos conhecimentos sobre termodinâmica e cinética química, e supondo a queima total de
HgO a 1 atm e a 300 K, assinale a alternativa correta.

No jornal O Estado de São Paulo, de 30 de agosto de 2011, foi publicada uma reportagem sobre o acidente nuclear na usina Daiichi, em Fukushima no Japão “[...] em 33 localidades havia um excesso de césio-137 de 1,48 milhão de becquerel por metro quadrado, [...]”.
Com base no texto acima e nos conceitos sobre processos radioativos, analise as afirmações a seguir.
I - O césio-137 é um material radioativo com tempo de meia vida curto e não apresenta risco à saúde das pessoas que moram na região afetada pelo acidente.
II- A partícula α possui estrutura semelhante ao núcleo do átomo de hélio.
III- Processos radioativos são essencialmente transformações nucleares, na qual núcleos instáveis emitem radiações.
IV- Bequerel é uma grandeza que mede a intensidade de radiação ou a atividade radioativa.
Assinale a alternativa correta.
No jornal O Estado de São Paulo, de 30 de agosto de 2011, foi publicada uma reportagem sobre o acidente nuclear na usina Daiichi, em Fukushima no Japão “[...] em 33 localidades havia um excesso de césio-137 de 1,48 milhão de becquerel por metro quadrado, [...]”.
Com base no texto acima e nos conceitos sobre processos radioativos, analise as afirmações a seguir.
I - O césio-137 é um material radioativo com tempo de meia vida curto e não apresenta risco à saúde das pessoas que moram na região afetada pelo acidente.
II- A partícula α possui estrutura semelhante ao núcleo do átomo de hélio.
III- Processos radioativos são essencialmente transformações nucleares, na qual núcleos instáveis emitem radiações.
IV- Bequerel é uma grandeza que mede a intensidade de radiação ou a atividade radioativa.
Baseado no texto e nas reações acima, juntamente com os conceitos químicos, analise as afirmações a seguir.
I- No cátodo o etanol é oxidado a etanal.
II- No ânodo ocorre uma reação de redução.
III- O sentido da corrente elétrica (i) é do ânodo para o cátodo.
IV- Na reação global corresponde a uma reação de combustão incompleta do etanol.
Assinale a alternativa correta.
Baseado no texto e nas reações acima, juntamente com os conceitos químicos, analise as afirmações a seguir.
I- No cátodo o etanol é oxidado a etanal.
II- No ânodo ocorre uma reação de redução.
III- O sentido da corrente elétrica (i) é do ânodo para o cátodo.
IV- Na reação global corresponde a uma reação de combustão incompleta do etanol.