Questõesde IF-TM sobre Química Orgânica
Entre os compostos orgânicos naturais encontram-se os glicídios, proteínas e os lipídios. Os glicídios são
compostos de função mista do tipo poliálcool-aldeído ou poliálcool-cetona e outros compostos que, por
hidrólise produzem poliálcool-aldeído e/ou poliálcool-cetona. As proteínas são polímeros cujas unidades
constituintes fundamentais são os aminoácidos. Os lipídios são formados por uma grande diversidade de
compostos orgânicos, entre os quais estão os óleos e gorduras comestíveis, e os cerídios. Os óleos e gorduras
comestíveis são constituídos por uma mistura na qual predominam os triésteres de ácidos graxos, e os
cerídios são monoésteres de ácidos graxos com álcoois superiores.
A seguir, estão representadas as fórmulas de alguns compostos orgânicos:

Com a leitura do texto, a observação das fórmulas acima e com os seus conhecimentos de química, é correto
afirmar que:

Sobre as substâncias citadas no texto é incorreto afirmar que:
Quando uma pessoa ingere bebidas alcoólicas, o álcool passa rapidamente para a corrente sanguínea, pela qual é
levado para todas as outras partes do corpo. O metabolismo do etanol no nosso organismo, principalmente no fígado,
ocorre em várias etapas catalisadas por enzimas. O esquema abaixo representa este processo de modo simplificado:
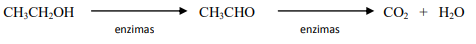
Disponível em: < http://qnesc.sbq.org.br/online/qnesc05/quimsoc.pdf > Acesso em: 1 nov. 2011 (adaptado).
Dadas as massas molares (g.mol-1): C = 12, H = 1, O = 16
De acordo com os seus conhecimentos de química é incorreto afirmar que:
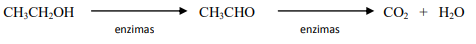
O gás hidrogênio é muito utilizado em diversos processos industriais, tais como: síntese de amônia,
hidrogenação de óleos e gorduras, etc. Uma das formas utilizadas para a produção do gás hidrogênio é a partir da
reação de reforma do metano. Este processo, em condições adequadas, ocorre através de duas reações
representadas pelas equações 1 e 2, já a equação 3 representa a reação global deste processo.
Equação 1: CH4(g) + H2O(g) → CO(g) + 3H2(g) ∆ H = +206 kJ
Equação 2: CO(g) + H2O(g) → CO2(g) + H2(g) ∆ H = - 41 kJ
Equação 3: CH4(g) + 2H2O(v) → CO2(g) + 4H2(g)
Dados: Massas molares (g.mol-1): C = 12, H = 1, O = 16
Sobre as substâncias e as reações representadas por estas equações é incorreto afirmar que:
O gás hidrogênio é muito utilizado em diversos processos industriais, tais como: síntese de amônia, hidrogenação de óleos e gorduras, etc. Uma das formas utilizadas para a produção do gás hidrogênio é a partir da reação de reforma do metano. Este processo, em condições adequadas, ocorre através de duas reações representadas pelas equações 1 e 2, já a equação 3 representa a reação global deste processo.
Equação 1: CH4(g) + H2O(g) → CO(g) + 3H2(g) ∆ H = +206 kJ
Equação 2: CO(g) + H2O(g) → CO2(g) + H2(g) ∆ H = - 41 kJ
Equação 3: CH4(g) + 2H2O(v) → CO2(g) + 4H2(g)
Dados: Massas molares (g.mol-1): C = 12, H = 1, O = 16
Sobre as substâncias e as reações representadas por estas equações é incorreto afirmar que: