23a070c7-e0
FATEC 2013 - Química - Soluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais., Soluções e Substâncias Inorgânicas
Analisando a tabela, conclui-se, corretamente, que a água é considerada.
Dados: densidade da solução=1g/cm3
ppm =partespormilhão
ppb=partesporbilhão
Analisando a tabela, conclui-se, corretamente, que a água é considerada.
Dados: densidade da solução=1g/cm3
ppm =partespormilhão
ppb=partesporbilhão
Dados: densidade da solução=1g/cm3
ppm =partespormilhão
ppb=partesporbilhão
Em depósitos subterrâneos, a água pode entrar em contato com certos materiais como o calcário (CaCO3 ) ou a dolomita (CaCO3 . MgCO3 ).
Dessa forma, passa a existir em sua composição uma quantidade excessiva de íons Ca2+ e Mg2+, passando a ser denominada água dura e tornando-a imprópria para consumo humano.
Na indústria, quando exposta ao aumento de temperatura, ocorre cristalização do calcário, criando incrustações que exigem altos custos para reparação e manutenção dos equipamentos, levando à menor produtividade e ao risco de explosões das caldeiras.
Considere a tabela de classificação da água.

Dessa forma, passa a existir em sua composição uma quantidade excessiva de íons Ca2+ e Mg2+, passando a ser denominada água dura e tornando-a imprópria para consumo humano.
Na indústria, quando exposta ao aumento de temperatura, ocorre cristalização do calcário, criando incrustações que exigem altos custos para reparação e manutenção dos equipamentos, levando à menor produtividade e ao risco de explosões das caldeiras.
Considere a tabela de classificação da água.

A
moderada, quando a concentração está entre 7,5 e 15 ppm (m/m)
B
moderada, quando a concentração está entre 75 e 150 ppb (m/m).
C
mole, quando a concentração está abaixo de 0,75 ppm (m/m).
D
dura, quando a concentração está acima de 150 ppm (m/m)
E
dura, quando a concentração está acima de 150 ppb (m/m).







 FUNÇÃO ORGÂNICA amida
FUNÇÃO ORGÂNICA amida FUNÇÃO ORGÂNICA aminoácido
FUNÇÃO ORGÂNICA aminoácido FUNÇÃO ORGÂNICA amina
FUNÇÃO ORGÂNICA amina FUNÇÃO ORGÂNICA ácido carboxílico
FUNÇÃO ORGÂNICA ácido carboxílico FUNÇÃO ORGÂNICA cetona
FUNÇÃO ORGÂNICA cetona






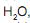 na qual os dois átomos de hidrogênio estão unidos ao átomo de oxigênio por ligações
na qual os dois átomos de hidrogênio estão unidos ao átomo de oxigênio por ligações


