Questõesde FATEC sobre Química
O radônio, símbolo Rn, pertencente à família dos gases
nobres, encontrado no grupo 18 ou 8A da tabela periódica
dos elementos, é usado na radioterapia e na composição
de cápsulas para aplicação em pacientes com câncer.
Certo isótopo desse elemento possui 86 prótons,
86 elétrons e número de massa 222, logo o número de
nêutrons desse isótopo é
A reação que ocorre para a formação do sal presente na
tabela é
A fórmula estrutural do composto orgânico com menor
ponto de ebulição presente na tabela dada é
O composto molecular gasoso, a 25°C e 1 atm, é
A platina é um metal nobre, encontrada livre na natureza
na forma de pepitas, e é muito empregada na produção
de catalisadores, que são utilizados para
Assim como qualquer atleta, um jogador de futebol deve tomar muitos cuidados em relação à sua dieta e hábitos
alimentares, pois o que ele ingere no dia a dia fará grande diferença para o rendimento nos treinos, para a recuperação do
corpo e nos dias de jogo.
Se o jogador não se organizar em relação à sua dieta e suplementação, poderá perder força, rendimento e velocidade
dentro do campo.
Uma alimentação balanceada deve apresentar alguns itens, como:
I. Carboidratos
II. Proteínas
III. Gorduras
IV. Vitaminas e Minerais
(http://www.anutricionista.com/como-deve-ser-o-cardapio-de-um-jogador-de-futebol.html Acesso em: 14.02.2014. Adaptado)
Considerando os quatro itens mencionados no texto, assinale a alternativa que exemplifica cada um deles, respectivamente.
I. C12H22O11
II. 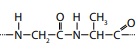
III. sódio
IV. 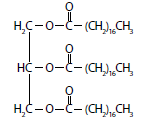
I. 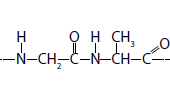
II. 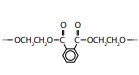
III. C12H22O11
IV. sódio
I. ferro
II. 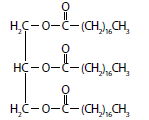
III. 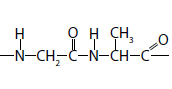
IV. C6 H12O6
I. 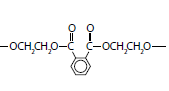
II. C6 H12O6
III. 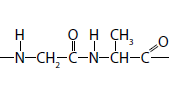
IV. ferro
I. C12H22O11
II. 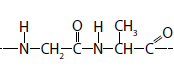
III. 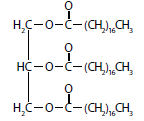
IV. ferro
Determinado veículo foi submetido à inspeção veicular ambiental obrigatória, para obter o licenciamento no município de São Paulo.
Nessa inspeção, após aprovado em uma verificação prévia que leva em conta vazamentos, estado do escapamento e condições de
ruído, o veículo passa por medições de marcha lenta e de emissão e diluição de gases, que devem estar dentro de certos limites. Os
limites para a emissão e diluição de gases valem também para o motor funcionando em alta rotação.
As tabelas I, II e III mostram os valores limites para o veículo em questão e os valores medidos.

Analisando-se esses dados, conclui-se que o veículo submetido à inspeção deve ter sido
As tabelas I, II e III mostram os valores limites para o veículo em questão e os valores medidos.

Analisando-se esses dados, conclui-se que o veículo submetido à inspeção deve ter sido
O monitoramento da qualidade do ar em São Paulo é realizado, diariamente, pela CETESB (Companhia Ambiental do Estado de São Paulo), a
fim de determinar o nível de concentração de um grupo de poluentes universalmente consagrados como indicadores.
Esses indicadores foram selecionados devido à sua maior frequência na atmosfera e também devido aos efeitos adversos que causam ao meio
ambiente. Para cada um deles, foram definidos padrões de qualidade do ar, ou seja, limites máximos de concentração que, quando ultrapassados,
podem afetar a saúde, a segurança e o bem-estar da população, bem como ocasionar danos ao meio ambiente em geral.
Assim, por exemplo, o estudo de um desses indicadores demonstrou que não se devem deixar veículos com o motor em funcionamento em
ambientes pouco ventilados, como garagens fechadas e túneis sem circulação adequada de ar, porque ele se combina com moléculas de
hemoglobina, inutilizando-as irreversivelmente para o transporte de oxigênio.
Esse indicador é um gás inodoro representado pela fórmula molecular
Esses indicadores foram selecionados devido à sua maior frequência na atmosfera e também devido aos efeitos adversos que causam ao meio ambiente. Para cada um deles, foram definidos padrões de qualidade do ar, ou seja, limites máximos de concentração que, quando ultrapassados, podem afetar a saúde, a segurança e o bem-estar da população, bem como ocasionar danos ao meio ambiente em geral.
Assim, por exemplo, o estudo de um desses indicadores demonstrou que não se devem deixar veículos com o motor em funcionamento em ambientes pouco ventilados, como garagens fechadas e túneis sem circulação adequada de ar, porque ele se combina com moléculas de hemoglobina, inutilizando-as irreversivelmente para o transporte de oxigênio.
Esse indicador é um gás inodoro representado pela fórmula molecular
O pigmento branco mais utilizado em tintas e em esmaltes é o dióxido de titânio, TiO2
. A porcentagem em massa de titânio nesse
pigmento é de
Massas molares em g/mol
Ti = 48
O = 16
Massas molares em g/mol
Ti = 48
O = 16
Uma das substâncias responsáveis pelo cheiro desagradável que as pessoas sentem, ao passarem nas proximidades de rios e de
córregos poluídos por esgoto, é o sulfeto de hidrogênio, H2S (g). Esse mau cheiro se intensifica principalmente em dias quentes, pois
o aumento de temperatura diminui a solubilidade desse gás em água.
Quando borbulhado em água, o H2S comporta-se como ácido fraco, estabelecendo-se os equilíbrios simultâneos representados pelas
equações a seguir:

Dentre os procedimentos a seguir, o único que provoca um aumento do escape de sulfeto de hidrogênio de uma solução aquosa para
o ar é
Quando borbulhado em água, o H2S comporta-se como ácido fraco, estabelecendo-se os equilíbrios simultâneos representados pelas equações a seguir:

Dentre os procedimentos a seguir, o único que provoca um aumento do escape de sulfeto de hidrogênio de uma solução aquosa para o ar é
O composto de nome ácido 2- acetoxibenzoico é o conhecido medicamento ácido acetilsalicílico.
Examinando-se esse nome, pode-se concluir que se trata de um
Há livros da famosa escritora Agatha Christie que fazem menção a crimes que foram cometidos com o uso de substâncias químicas.
Em O misterioso caso de Styles, é citada a substância hidrocloreto de estricnina, extremamente venenosa, cuja solubilidade
em água é cerca de 1 g / 40 mL. Sabendo-se que a massa molar dessa substância é aproximadamente 400 g / mol, calcula-se que a
solubilidade em água do veneno em questão, expressa em mol / L, seja da ordem de
Considerando as substâncias químicas empregadas na construção do eletrodo fotocatalítico, o qual permite a
realização da fotossíntese artificial, pode-se notar que há uma substância simples, formada por átomos de um
único elemento químico, e substâncias compostas, formadas por átomos de mais de um elemento químico.
A única substância simples empregada nesse eletrodo é
Considerando as substâncias químicas empregadas na construção do eletrodo fotocatalítico, o qual permite a realização da fotossíntese artificial, pode-se notar que há uma substância simples, formada por átomos de um único elemento químico, e substâncias compostas, formadas por átomos de mais de um elemento químico.
A única substância simples empregada nesse eletrodo é
Fotossíntese artificial gera hidrogênio para células a combustível
Redação do Site Inovação Tecnológica - 18/02/2010
Fontes de energia do futuro
Células a combustível alimentadas por hidrogênio e por energia solar são as duas maiores esperanças para as fontes de energia do futuro, por serem mais amigáveis ambientalmente e, sobretudo, sustentáveis.
A combinação das duas, então, é considerada como particularmente limpa: produzir hidrogênio para alimentar as células a combustível, quebrando moléculas de água com a luz solar, seria de fato o melhor dos mundos.
Esta é a chamada fotossíntese artificial, que vem sendo alvo de pesquisas de vários grupos de cientistas, ao redor do mundo.
Eletrodo fotocatalítico
Uma equipe liderada por Thomas Nann e Christopher Pickett, da Universidade de East Anglia, no Reino Unido, criou um fotoeletrodo eficiente, robusto, que pode ser fabricado com materiais comuns e de baixo custo.
O novo sistema consiste de um eletrodo de ouro que é recoberto com camadas formadas por nanopartículas de fosfeto de índio (InP). A esse eletrodo, os pesquisadores adicionaram um composto de ferro-enxofre [Fe2 S2 (CO)6 ] sobre as camadas.
Quando submerso em água e iluminado com a luz do Sol, sob uma corrente elétrica relativamente fraca, este sistema fotoeletrocatalítico produz hidrogênio com uma eficiência de 60%.
(
Uma forma de evitar a poluição ambiental causada
pelo descarte de óleo de cozinha usado é
reaproveitá-lo para produzir sabões, que são sais
de ácidos carboxílicos. Para tanto, faz-se reagir o
óleo com solução aquosa fortemente alcalina de
NaOH e/ou KOH.
Nessa reação, conhecida como reação de
saponificação, forma-se também um outro produto
que é o
Uma forma de evitar a poluição ambiental causada pelo descarte de óleo de cozinha usado é reaproveitá-lo para produzir sabões, que são sais de ácidos carboxílicos. Para tanto, faz-se reagir o óleo com solução aquosa fortemente alcalina de NaOH e/ou KOH.
Nessa reação, conhecida como reação de saponificação, forma-se também um outro produto que é o
No inverno de 2010, a umidade relativa do ar, na capital e em vários municípios do interior do Estado de São
Paulo, atingiu níveis muito baixos, semelhantes aos encontrados em desertos, e as temperaturas, durante
vários dias, estiveram acima das médias para essa época do ano. Nesses dias muito secos e quentes, além
dos danos à saúde, alguns outros fatos corriqueiros puderam ser observados. Assinale a alternativa que
identifica um desses fatos.
A cor das flores de diversas plantas ocorre devido à presença de substâncias, como as antocianinas, que
atuam como indicadores ácido-base. Assim, conforme o pH do solo, a cor das flores pode variar. É o caso das
hortênsias, que apresentam cor azul em solos ácidos e rosa em solos alcalinos.
Caso uma pessoa queira cultivar hortênsias de cor rosa, em um jardim cujo solo seja ácido, ela deverá corrigir
o pH e, para isso, poderá misturar à terra, em quantidade adequada,
A cor das flores de diversas plantas ocorre devido à presença de substâncias, como as antocianinas, que atuam como indicadores ácido-base. Assim, conforme o pH do solo, a cor das flores pode variar. É o caso das hortênsias, que apresentam cor azul em solos ácidos e rosa em solos alcalinos.
Caso uma pessoa queira cultivar hortênsias de cor rosa, em um jardim cujo solo seja ácido, ela deverá corrigir o pH e, para isso, poderá misturar à terra, em quantidade adequada,
Um veículo de passeio, movido a gasolina, deixou a capital paulista com o tanque cheio, dirigindo-se a uma
cidade do interior situada a 480 km, na região noroeste do estado. Ao final da viagem, verificou-se que o
consumo médio do veículo foi de 16 km por litro de combustível.
Admitindo-se que a composição média da gasolina seja dada pela fórmula C8
H18 e que a combustão seja
completa, conclui-se que o volume de CO2
, em litros, medido nas CATP e lançado ao ar durante a viagem foi
de, aproximadamente,
Dados
Volume molar de gás nas CATP = 25 L / mol
Densidade da gasolina = 8 x 102 g / L
Massas molares em g / mol:
C = 12; H = 1 e O = 16
Um veículo de passeio, movido a gasolina, deixou a capital paulista com o tanque cheio, dirigindo-se a uma cidade do interior situada a 480 km, na região noroeste do estado. Ao final da viagem, verificou-se que o consumo médio do veículo foi de 16 km por litro de combustível.
Admitindo-se que a composição média da gasolina seja dada pela fórmula C8 H18 e que a combustão seja completa, conclui-se que o volume de CO2 , em litros, medido nas CATP e lançado ao ar durante a viagem foi de, aproximadamente,
Dados
Volume molar de gás nas CATP = 25 L / mol
Densidade da gasolina = 8 x 102 g / L
Massas molares em g / mol:
C = 12; H = 1 e O = 16
Os elementos cloro (Z = 17) e iodo (Z = 53) pertencem ao mesmo grupo da tabela periódica. Assim, átomos
neutros desses elementos apresentam igual
I. número de prótons;
II. número de elétrons na camada de valência;
III. eletronegatividade.
É correto o que se afirma em
Os elementos cloro (Z = 17) e iodo (Z = 53) pertencem ao mesmo grupo da tabela periódica. Assim, átomos neutros desses elementos apresentam igual
I. número de prótons;
II. número de elétrons na camada de valência;
III. eletronegatividade.
É correto o que se afirma em