Analise a tabela, que mostra a composição de alguns minerais de ferro.
Mineral Composição Massa molar (g/mol)
goethita Fe2O3 . H2O 178hematita Fe2O3 160
pirita FeS2 120
siderita FeCO3 116
Os minerais que apresentam maior e menor porcentagem em
massa de ferro são, respectivamente,
Mineral Composição Massa molar (g/mol)
goethita Fe2O3 . H2O 178
pirita FeS2 120
siderita FeCO3 116
Os minerais que apresentam maior e menor porcentagem em massa de ferro são, respectivamente,
 e o átomo
e o átomo 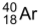 apresentam o mesmo número
apresentam o mesmo número
 , é isótono do átomo de túlio, Tm,
que possui 69 prótons e 100 nêutrons no núcleo.
, é isótono do átomo de túlio, Tm,
que possui 69 prótons e 100 nêutrons no núcleo.
 são isótopos do hidrogênio.
são isótopos do hidrogênio. são elementos isóbaros.
são elementos isóbaros. são elementos isótonos.
são elementos isótonos.