a148a684-ab
ENEM 2023 - Química - Equilíbrio Químico, Soluções e Substâncias Inorgânicas, Substâncias e suas propriedades
Um assistente de laboratório precisou descartar sete frascos contendo solução de nitrato de mercúrio(I) que não
foram utilizados em uma aula prática. Cada frasco continha 5,25 g de Hg2
(NO3
)2
dissolvidos em água. Temendo a
toxidez do mercúrio e sabendo que o Hg2Cl2
tem solubilidade muito baixa, o assistente optou por retirar o mercúrio da
solução por precipitação com cloreto de sódio (NaCl), conforme a equação química:
Hg2(NO3
)2 (aq) + 2 NaCl (aq) ➝ Hg2Cl2 (s) + 2 NaNO3 (aq)
Na dúvida sobre a massa de NaCl a ser utilizada, o assistente aumentou gradativamente a quantidade adicionada
em cada frasco, como apresentado no quadro.
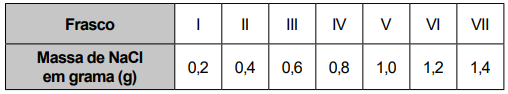
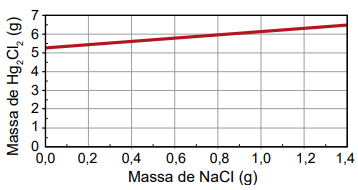
O produto obtido em cada experimento foi filtrado, secado e teve sua massa aferida. O assistente organizou os
resultados na forma de um gráfico que correlaciona a massa de NaCl adicionada com a massa de Hg2Cl2
obtida em
cada frasco. A massa molar do Hg2
(NO3
)2
é 525 g mol–1, a do NaCl é 58 g mol–1 e a do Hg2Cl2
é 472 g mol–1.
Qual foi o gráfico obtido pelo assistente de laboratório?
Um assistente de laboratório precisou descartar sete frascos contendo solução de nitrato de mercúrio(I) que não
foram utilizados em uma aula prática. Cada frasco continha 5,25 g de Hg2
(NO3
)2
dissolvidos em água. Temendo a
toxidez do mercúrio e sabendo que o Hg2Cl2
tem solubilidade muito baixa, o assistente optou por retirar o mercúrio da
solução por precipitação com cloreto de sódio (NaCl), conforme a equação química:
Hg2(NO3
)2 (aq) + 2 NaCl (aq) ➝ Hg2Cl2 (s) + 2 NaNO3 (aq)
Na dúvida sobre a massa de NaCl a ser utilizada, o assistente aumentou gradativamente a quantidade adicionada
em cada frasco, como apresentado no quadro.

O produto obtido em cada experimento foi filtrado, secado e teve sua massa aferida. O assistente organizou os
resultados na forma de um gráfico que correlaciona a massa de NaCl adicionada com a massa de Hg2Cl2
obtida em
cada frasco. A massa molar do Hg2
(NO3
)2
é 525 g mol–1, a do NaCl é 58 g mol–1 e a do Hg2Cl2
é 472 g mol–1.
Qual foi o gráfico obtido pelo assistente de laboratório?
A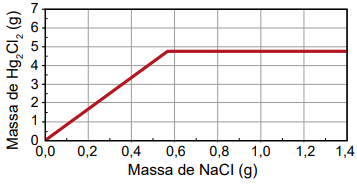

B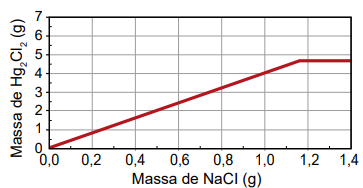

C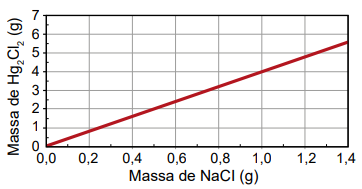

D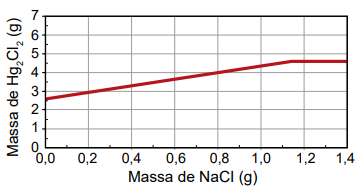

E