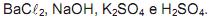65eb0451-fc
USP 2010 - Química - Soluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais., Equilíbrio Químico, Sistemas Homogêneos: Equilíbrio Químico na Água: pH e pOH, Indicadores Ácido-Base, Solução Tampão., Soluções e Substâncias Inorgânicas
Considere 4 frascos, cada um contendo diferentes substâncias, a saber:
Frasco 1: 100 mL de H2O( L )
Frasco 2: 100 mL de solução aquosa de ácido acético de concentração 0,5 mol/L
Frasco 3: 100 mL de solução aquosa de KOH de concentração 1,0 mol/L
Frasco 4: 100 mL de solução aquosa de  de concentração 1,2 mol/L
de concentração 1,2 mol/L

Considere 4 frascos, cada um contendo diferentes substâncias, a saber:
Frasco 1: 100 mL de H2O( L )
Frasco 2: 100 mL de solução aquosa de ácido acético de concentração 0,5 mol/L
Frasco 3: 100 mL de solução aquosa de KOH de concentração 1,0 mol/L
Frasco 4: 100 mL de solução aquosa de de concentração 1,2 mol/L
de concentração 1,2 mol/L

Frasco 1: 100 mL de H2O( L )
Frasco 2: 100 mL de solução aquosa de ácido acético de concentração 0,5 mol/L
Frasco 3: 100 mL de solução aquosa de KOH de concentração 1,0 mol/L
Frasco 4: 100 mL de solução aquosa de
 de concentração 1,2 mol/L
de concentração 1,2 mol/L
A
nas soluções dos frascos 1, 2 e 4.
B
nas soluções dos frascos 1 e 3.
C
nas soluções dos frascos 2 e 4.
D
na solução do frasco 3.
E
na solução do frasco 4.






 será extraído do
será extraído do  pela água, até que a concentração de
pela água, até que a concentração de em
em  se iguale a zero.
se iguale a zero. será extraído da água pelo
será extraído da água pelo  até que a concentração de
até que a concentração de em água se iguale a zero.
em água se iguale a zero. no
no tenderá a aumentar e a de
tenderá a aumentar e a de na água, tenderá a diminuir, até que se atinja um estado de equilíbrio.
na água, tenderá a diminuir, até que se atinja um estado de equilíbrio. na água tenderá a aumentar e a de
na água tenderá a aumentar e a de  no
no , tenderá a diminuir, até que se atinja um estado de equilíbrio.
, tenderá a diminuir, até que se atinja um estado de equilíbrio. nas duas fases.
nas duas fases. sendo que 1 g de
sendo que 1 g de


 e
e
 e
e