83f6375e-4a
UFRN 2009, UFRN 2009, UFRN 2009 - Química - Relações da Química com as Tecnologias, a Sociedade e o Meio Ambiente
Os radicais l ivres têm funções importantes no organismo humano. Não obstante, em excesso eles podem ser prejudiciais, pois danificam as células e o material genético (alteram o DNA). Uma vez formados, os radicais l ivres desencadeiam reações que se propagam a grande velocidade, em conseqüência da alta reatividade.
O comportamento químico dos radicais livres se expl ica pelo fato de eles serem estruturas com
Os radicais l ivres têm funções importantes no organismo humano. Não obstante, em excesso eles podem ser prejudiciais, pois danificam as células e o material genético (alteram o DNA). Uma vez formados, os radicais l ivres desencadeiam reações que se propagam a grande velocidade, em conseqüência da alta reatividade.
O comportamento químico dos radicais livres se expl ica pelo fato de eles serem estruturas com
O comportamento químico dos radicais livres se expl ica pelo fato de eles serem estruturas com
A
uma carga total negativa.
B
todos os elétrons emparelhados.
C
uma carga total positiva.
D
um elétron desemparelhado.
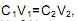 o volume inicial de solução de NaOH 1 mol/L retirado para se obter a solução di luída corresponderá a:
o volume inicial de solução de NaOH 1 mol/L retirado para se obter a solução di luída corresponderá a: 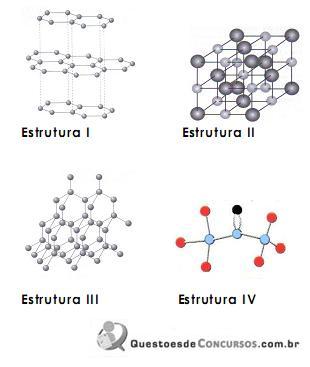

 como acelga, soja e cacau, dificultam a absorção dos íons Ca 2+ pelo intestino.
como acelga, soja e cacau, dificultam a absorção dos íons Ca 2+ pelo intestino.
 deslocando o equilíbrio para os produtos.
deslocando o equilíbrio para os produtos. deslocando o equilíbrio para os reagentes.
deslocando o equilíbrio para os reagentes. desloca o equilíbrio, aumentando a quantidade de
desloca o equilíbrio, aumentando a quantidade de 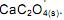
 desloca o equilíbrio no sentido de aumentar a quantidade de Ca 2+ (aq)
desloca o equilíbrio no sentido de aumentar a quantidade de Ca 2+ (aq)
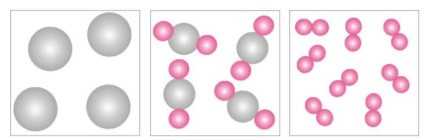


 e NaOH, o sódio possui
e NaOH, o sódio possui 