869609d2-df
UFRN 2009, UFRN 2009, UFRN 2009 - Química - Equilíbrio Químico, Sistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores.
Nutricionistas têm afirmado que alimentos
ricos em ácido oxálico (H2C2O4), como
acelga, soja e cacau, dificultam a absorção
dos íons Ca2+ pelo intestino.
Considere a informação acima e o equilíbrio
a seguir:
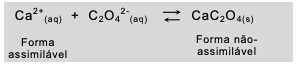
Esse equilíbrio está relacionado com as
formas do cálcio assimilável pelo intestino
humano e com as do não-assimilável.
Uma quantidade elevada de alimentos ricos
em oxalato dificulta a absorção de Ca2+
porque
Nutricionistas têm afirmado que alimentos
ricos em ácido oxálico (H2C2O4), como
acelga, soja e cacau, dificultam a absorção
dos íons Ca2+ pelo intestino.
Considere a informação acima e o equilíbrio
a seguir:

Esse equilíbrio está relacionado com as
formas do cálcio assimilável pelo intestino
humano e com as do não-assimilável.
Uma quantidade elevada de alimentos ricos
em oxalato dificulta a absorção de Ca2+
porque
A
o ácido oxálico reage com os íons C2O4 2- (aq), deslocando o equilíbrio para os produtos.
B
o ácido oxálico dissolve o CaC2O4(s), deslocando o equilíbrio para os reagentes.
C
o aumento da concentração dos íons oxalato (C2O4 2- (aq)) desloca o equilíbrio, aumentando a quantidade de CaC2O4(s).
D
o aumento da concentração íons (C2O4 2- (aq)) desloca o equilíbrio no sentido de aumentar a quantidade de Ca2+ (aq).



