5b8749d3-5e
UFMG 2008 - Química - Cinética Química, Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador, Transformações Químicas e Energia, Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess.
O propeno,  ao reagir com o brometo de hidrogênio, HBr, produz uma mistura de dois compostos ? o brometo de n-propila,
ao reagir com o brometo de hidrogênio, HBr, produz uma mistura de dois compostos ? o brometo de n-propila,  e o brometo de isopropila,
e o brometo de isopropila, 
As reações responsáveis pela formação desses compostos estão representadas nestas duas equações:

Sabe-se que a velocidade da reação II é maior que a da reação I.
Comparando-se essas duas reações, é CORREtO afrmar que, na II,
O propeno,  ao reagir com o brometo de hidrogênio, HBr, produz uma mistura de dois compostos ? o brometo de n-propila,
ao reagir com o brometo de hidrogênio, HBr, produz uma mistura de dois compostos ? o brometo de n-propila,  e o brometo de isopropila,
e o brometo de isopropila, 
As reações responsáveis pela formação desses compostos estão representadas nestas duas equações:

Sabe-se que a velocidade da reação II é maior que a da reação I.
Comparando-se essas duas reações, é CORREtO afrmar que, na II,
 ao reagir com o brometo de hidrogênio, HBr, produz uma mistura de dois compostos ? o brometo de n-propila,
ao reagir com o brometo de hidrogênio, HBr, produz uma mistura de dois compostos ? o brometo de n-propila,  e o brometo de isopropila,
e o brometo de isopropila, 
As reações responsáveis pela formação desses compostos estão representadas nestas duas equações:

Sabe-se que a velocidade da reação II é maior que a da reação I.
Comparando-se essas duas reações, é CORREtO afrmar que, na II,
A
a energia de ativação é maior.
B
a energia do estado de transição é menor.
C
a energia dos reagentes é maior.
D
a energia liberada na forma de calor é menor.
 , impura, com massa de 2,53 g, é dissolvida em água. A solução resultante é, então, tratada com cloreto de bário,
, impura, com massa de 2,53 g, é dissolvida em água. A solução resultante é, então, tratada com cloreto de bário,  , em excesso. Nessa reação, obtêm-se 2,33 g de sulfato de bário,
, em excesso. Nessa reação, obtêm-se 2,33 g de sulfato de bário, 


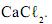 .
. 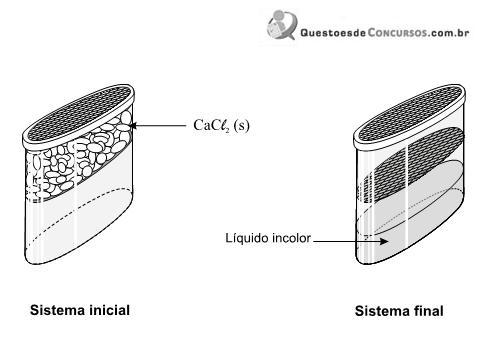
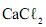 passa por um processo de sublimação.
passa por um processo de sublimação.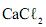 tem seu retículo cristalino quebrado.
tem seu retículo cristalino quebrado.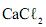 .
.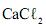 .
. , etanol,
, etanol,  e tetracloreto de carbono,
e tetracloreto de carbono,  :
:
 apresenta maior pressão de vapor
apresenta maior pressão de vapor apresenta menor temperatura de ebulição.
apresenta menor temperatura de ebulição.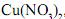 , uma de nitrato de magnésio,
, uma de nitrato de magnésio, , e uma de nitrato de zinco,
, e uma de nitrato de zinco,  .
. 

 que, de acordo com a situação, apresenta duas cores distintas — azul ou rosa —, como representado nesta equação:
que, de acordo com a situação, apresenta duas cores distintas — azul ou rosa —, como representado nesta equação:

 liberada na queima do combustível.
liberada na queima do combustível. 
 produzido é o
produzido é o 










 (aq), adicionou-se água pura, em quantidade sufciente para se obterem 100,0 mL de solução diluída.
(aq), adicionou-se água pura, em quantidade sufciente para se obterem 100,0 mL de solução diluída.
 observou-se, durante a dissolução, um resfriamento do sistema
observou-se, durante a dissolução, um resfriamento do sistema aumenta a energia cinética média das moléculas da água.
aumenta a energia cinética média das moléculas da água. dissolvida determina o grau de resfriamento do sistema.
dissolvida determina o grau de resfriamento do sistema. é um processo exotérmico.
é um processo exotérmico.

 (g) foram adicionados a um recipiente, que, imediatamente, foi fechado e mantido em temperatura constante.
(g) foram adicionados a um recipiente, que, imediatamente, foi fechado e mantido em temperatura constante.  (g) se decompôs, transformando-se em
(g) se decompôs, transformando-se em  (g) e
(g) e 
 em mol, variou com o tempo, até o sistema alcançar o equilíbrio, como mostrado neste quadro:
em mol, variou com o tempo, até o sistema alcançar o equilíbrio, como mostrado neste quadro:
 a pressão do sistema é maior que em
a pressão do sistema é maior que em  .
.
 são azuis e que as de nitrato de zinco (II),
são azuis e que as de nitrato de zinco (II),  são incolores.
são incolores.  na concentração de 1 mol/L, foi armazenado durante um ano.
na concentração de 1 mol/L, foi armazenado durante um ano.