b60ae870-a9
UECE 2022 - Química - Transformações Químicas e Energia
A desintegração radioativa que ocorre observando as leis
de Frederic Soddy (1877 – 1956) e Kasimierz Fajans (1887 – 1975),
iniciando com 92U235 e finalizando em 82Pb207, emite
A desintegração radioativa que ocorre observando as leis
de Frederic Soddy (1877 – 1956) e Kasimierz Fajans (1887 – 1975),
iniciando com 92U235 e finalizando em 82Pb207, emite
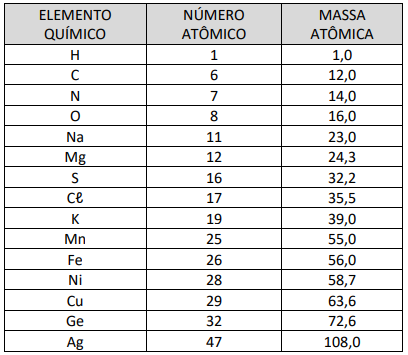
DADOS QUE PODEM SER USADOS NESTA PROVA

A
7 partículas alfa e 4 partículas beta.
B
8 partículas alfa e 7 partículas beta.
C
7 partículas alfa e 2 partículas beta
D
8 partículas alfa e 4 partículas beta
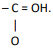

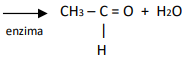 .
.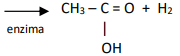 .
.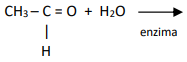 CH
CH CH3 – O – CH3 + [O]
CH3 – O – CH3 + [O]