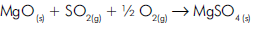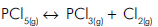dea7981a-e1
UCPEL 2007 - Química - Transformações Químicas e Energia, Fórmulas, Balanceamento e Leis ponderais das reações químicas, Eletroquímica: Oxirredução, Potenciais Padrão de Redução, Pilha, Eletrólise e Leis de Faraday., Representação das transformações químicas
Na reação representada pela equação:
 após o balanceamento, o coeficiente do agente oxidante
será
após o balanceamento, o coeficiente do agente oxidante
será
Na reação representada pela equação: após o balanceamento, o coeficiente do agente oxidante
será
após o balanceamento, o coeficiente do agente oxidante
será
A
8
B
3
C
5
D
2
E
1