d71dc49c-49
UFRN 2010, UFRN 2010, UFRN 2010 - Química - Teoria Atômica: átomos e sua estrutura - número atômico, número de massa, isótopos, massa atômica, Transformações Químicas
Leia o texto abaixo.

O teste descrito no texto se baseia na propriedade dos átomos de carbono conhecida como
Leia o texto abaixo.

O teste descrito no texto se baseia na propriedade dos átomos de carbono conhecida como

O teste descrito no texto se baseia na propriedade dos átomos de carbono conhecida como
A
isotopia.
B
isomeria.
C
isotonia.
D
isobaria.

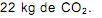

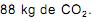

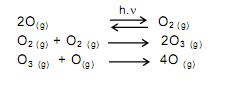
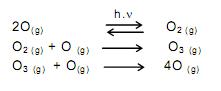
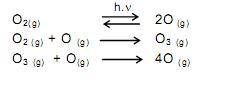
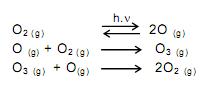


 o volume de nitrogênio gasoso que se obtém é, aproximadamente, de
o volume de nitrogênio gasoso que se obtém é, aproximadamente, de 
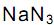 , o volume de nitrogênio gasoso que se obtém é, aproximadamente, de
, o volume de nitrogênio gasoso que se obtém é, aproximadamente, de 

 o volume de nitrogênio gasoso que se obtém é, aproximadamente,
o volume de nitrogênio gasoso que se obtém é, aproximadamente, e NaOH, o sódio possui
e NaOH, o sódio possui 

 e NaOH, o sódio possui
e NaOH, o sódio possui 