462875e9-e3
UEM 2010 - Química - Transformações Químicas e Energia, Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess.
Dadas as reações abaixo, assinale o que for correto.
H3BO3(aq) ==> HBO2(aq) + H2O(l) ∆H = -2,30 kJH2B4O7(aq) + H2O(l) ==> 4HBO2(aq) ∆H = -14,5 kJH2B4O7(aq) ==> 2B2O3(s) + H2O(l) ∆H = +22,7 kJ
A reação 2B2O3(S) + 2H2O(l) ==> 4HBO2(aq) é
endotérmica.
Dadas as reações abaixo, assinale o que for correto.
H3BO3(aq) ==> HBO2(aq) + H2O(l) ∆H = -2,30 kJ
H2B4O7(aq) + H2O(l) ==> 4HBO2(aq) ∆H = -14,5 kJ
H2B4O7(aq) ==> 2B2O3(s) + H2O(l) ∆H = +22,7 kJ
A reação 2B2O3(S) + 2H2O(l) ==> 4HBO2(aq) é endotérmica.
A reação 2B2O3(S) + 2H2O(l) ==> 4HBO2(aq) é endotérmica.
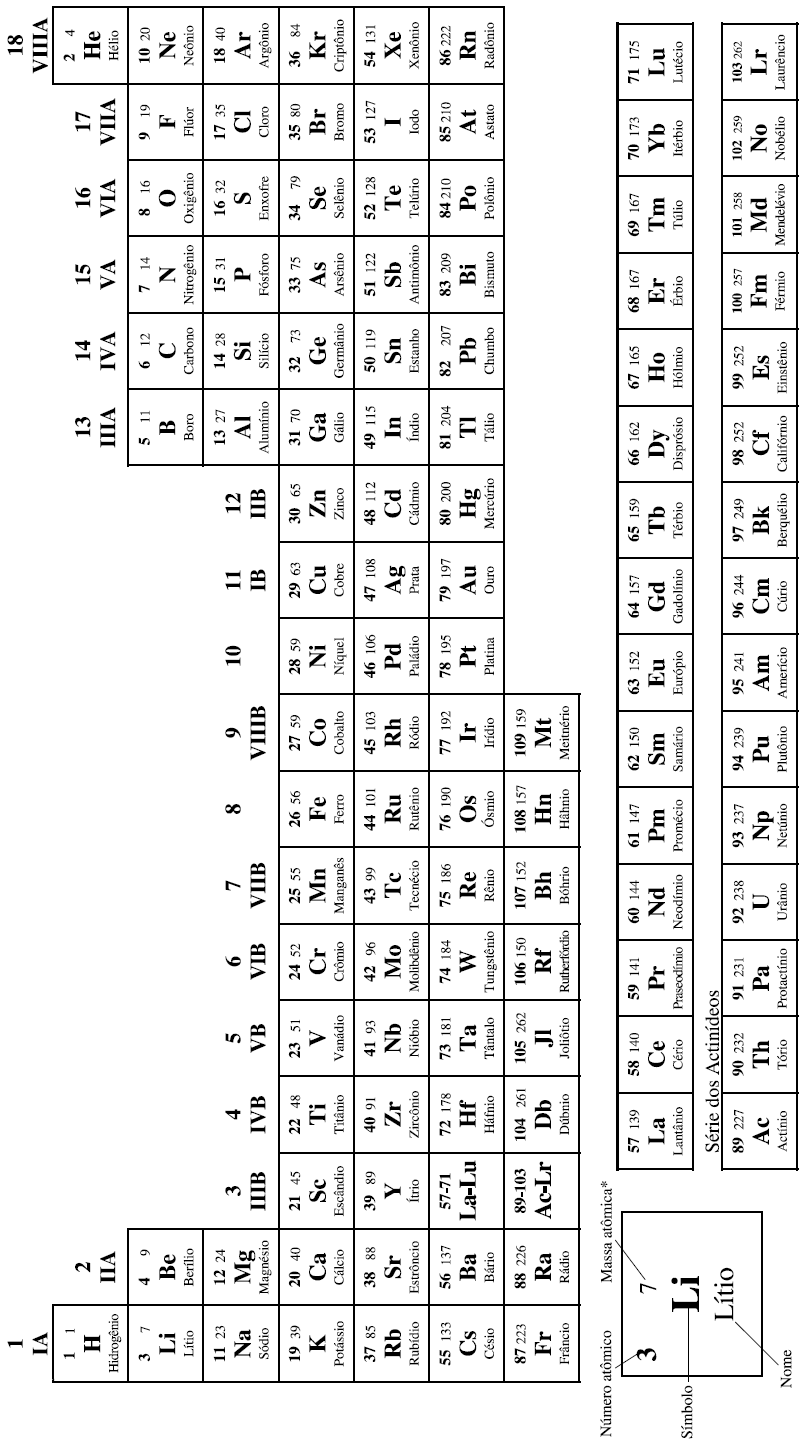
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
C
Certo
E
Errado