O íon potássio, K1+, apresenta maior raio que o
seu átomo neutro.
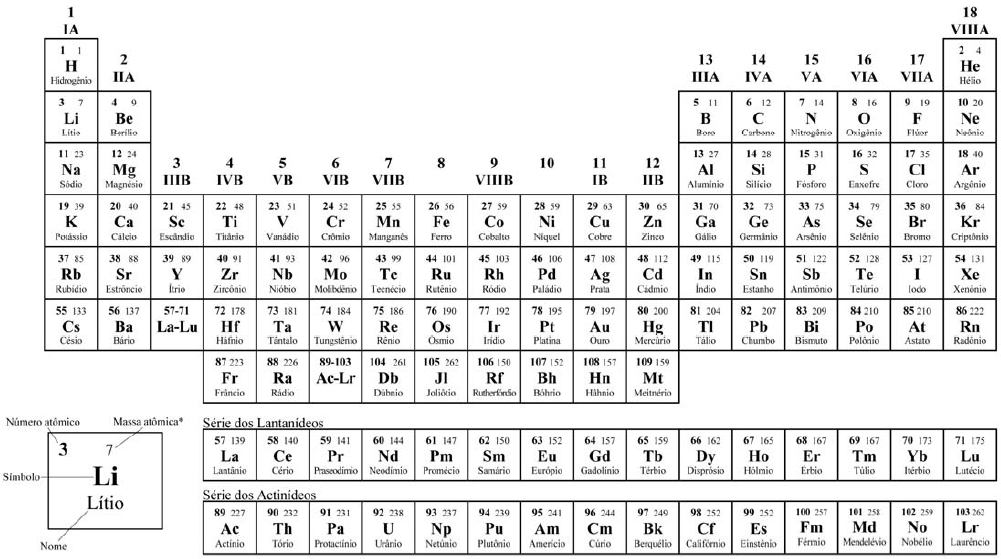
*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Com o auxílio das informações a seguir, sobre três dos elementos do Grupo 1 da Tabela Periódica, assinale a alternativa correta.
Elementos Raio atômico (nm) 1.ª Energia de Ionização (kJ/mol)
Li 0,123 520,0
Na 0,157 496,0
K 0,203 419,0



