O hidróxido de cálcio, Ca(OH)2
, pode ser neutralizado com H2
SO4
, de acordo com a equação química balanceada representada a seguir:
H2
SO4 (aq) + Ca(OH)2 (aq) → CaSO4 (aq) + 2 H2
O(l)
A respeito das espécies químicas que participam dessa reação de neutralização, verifica-se que o
O hidróxido de cálcio, Ca(OH)2 , pode ser neutralizado com H2 SO4 , de acordo com a equação química balanceada representada a seguir:
H2 SO4 (aq) + Ca(OH)2 (aq) → CaSO4 (aq) + 2 H2 O(l)
A respeito das espécies químicas que participam dessa reação de neutralização, verifica-se que o
 H2CO3 (aq)
H2CO3 (aq)
 HCO3-(aq) + H3O+(aq)
HCO3-(aq) + H3O+(aq) CO32-(aq) + H3O+(aq)
CO32-(aq) + H3O+(aq)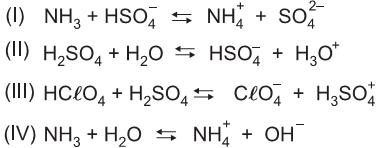
 é base em (I) e ácido em (II).
é base em (I) e ácido em (II).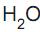 é base em (II) e ácido em (IV).
é base em (II) e ácido em (IV).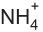 é base em (I) e ácido em (IV).
é base em (I) e ácido em (IV).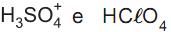 são respectivamente o ácido e a base conjugados de um sistema em (III).
são respectivamente o ácido e a base conjugados de um sistema em (III).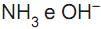 são respectivamente o ácido e a base conjugados de um sistema em (IV)
são respectivamente o ácido e a base conjugados de um sistema em (IV)