Questõesde UNICAMP sobre Soluções e Substâncias Inorgânicas
O aumento dos casos da Covid-19 provocou a escassez de
álcool etílico em gel no comércio, o que fez a população
buscar outros tipos de álcool para se prevenir. No entanto,
as opções de álcool disponíveis não eram eficazes. O
recomendado é o álcool 70° INPM (% massa/massa). As
opções de álcool disponíveis comercialmente à época da
escassez aparecem na tabela abaixo.
Tipo de álcool Concentração INPM (%massa/massa) Absoluto 99,6 Hidratado 92,6
Combustível 92,5
Limpeza 46,0
Para produzir álcool 70° INPM a partir dos outros tipos
disponíveis comercialmente, uma opção possível seria
misturar
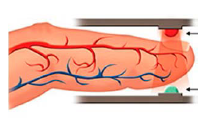
O oxímetro é usado na
triagem para a Covid-19.
Acoplado ao dedo, ele
emite luz em dois
comprimentos de onda
(660 nm e 940 nm) e mede
a quantidade de luz
absorvida (A) em cada caso. A partir disso, determina a
concentração percentual de oxi-hemoglobina (HbO2) e de
desoxi-hemoglobina (Hb) no sangue. Valores entre 95 e
100% para HbO2 indicam normalidade. Simplificadamente,
as quantidades de luz absorvidas em cada comprimento de
onda (A) se relacionam matematicamente às
concentrações [HbO2] e [Hb] conforme as seguintes
equações:
Hb (aq) + O2 (aq) ➝ HbO2 (aq)
A (em 660 nm) = 320 [HbO2] + 3227 [Hb]
A (em 940 nm)= 1214 [HbO2] + 693 [Hb].
Considere que uma pessoa tenha chegado ao hospital com
baixa saturação de O2 no sangue e, depois de submetida à
oxigenoterapia, começa a ter a saturação normalizada. Em
relação às medidas iniciais, quando a saturação de O2
começa a subir, a absorção de luz indicada pelo oxímetro

Massas molares em g mol-1: Na = 23; Mg = 24; Cl = 35,5; K = 39; Ca = 40.
Imagine-se como um dos coautores de um trabalho científico sobre a capacidade de dessalinização de fibras de carbono poroso (PCF). Ao revisar os dados da pesquisa, você observa que os resultados apresentados no gráfico a seguir estão consistentes para MgCl2 e CaCl2, do ponto de vista do conhecimento químico.
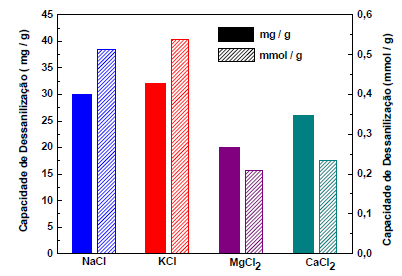
No entanto, você também observa no gráfico que a apresentação dos dados está

Episódios recentes de erupções vulcânicas têm trazido
consequências trágicas para a sociedade e para o meio
ambiente. Ativo desde 1983, o Vulcão Kilauea apresentou,
em 2018, a sua maior erupção já registrada. Quase ao
mesmo tempo, foi a vez do Vulcão Fuego da Guatemala
mostrar sua força. No Kilauea não houve explosões, ao
contrário do que ocorreu no Fuego. Os especialistas
afirmam que a ocorrência de uma erupção explosiva
depende da concentração e do tipo de gases dissolvidos
no magma, como SO2, HF e HCl, além de vapor de água e
CO2 aprisionados. A figura a seguir dá informações sobre a
relação entre quantidades (em mol) de SO2, HF e HCl no
magma de três vulcões distintos.

De acordo com a figura, em relação às quantidades de
gases dissolvidos no magma, é correto afirmar que as
concentrações de SO2 são maiores que as de HF e de HCl

Dois estudantes, de massa corporal em torno de 75 kg, da
Universidade de Northumbria, no Reino Unido, quase
morreram ao participar de um experimento científico no
qual seriam submetidos a determinada dose de cafeína e a
um teste físico posterior. Por um erro técnico, ambos
receberam uma dose de cafeína 100 vezes maior que a
dose planejada. A dose planejada era de 0,3 g de cafeína,
equivalente a três xícaras de café. Sabe-se que a União
Europeia, onde o teste ocorreu, classifica a toxicidade de
uma dada substância conforme tabela a seguir.

Considerando que a DL50 – dose necessária de uma dada
substância para matar 50% de uma população – da cafeína
é de 192 mg/kg, no teste realizado a dose aplicada foi
cerca de

Fake News ou não? Hoje em dia, a disponibilidade de
informações é muito grande, mas precisamos saber
interpretá-las corretamente. Um artigo na internet tem o
seguinte título: “Glutamato monossódico, o sabor que
mata!”. Em determinado ponto do texto, afirma-se:
“Só para você ter ideia dos riscos, organizações
internacionais de saúde indicam que a ingestão diária de
sódio para cada pessoa seja de 2,3 gramas. O glutamato é
composto por 21% de sódio e, com certeza, não será o
único tempero a ser acrescentado ao seu almoço ou jantar.
Além disso, o realçador (glutamato) só conta um terço do
nutriente que é encontrado no sal de cozinha.”
Dados de massas molares em g·mol-1
: sódio = 23, cloreto =
35,5, glutamato monossódico = 169.
Para tornar a argumentação do artigo mais consistente do
ponto de vista químico, você sugeriria a seguinte reescrita
dos trechos destacados:
Fake News ou não? Hoje em dia, a disponibilidade de informações é muito grande, mas precisamos saber interpretá-las corretamente. Um artigo na internet tem o seguinte título: “Glutamato monossódico, o sabor que mata!”. Em determinado ponto do texto, afirma-se:
“Só para você ter ideia dos riscos, organizações internacionais de saúde indicam que a ingestão diária de sódio para cada pessoa seja de 2,3 gramas. O glutamato é composto por 21% de sódio e, com certeza, não será o único tempero a ser acrescentado ao seu almoço ou jantar.
Além disso, o realçador (glutamato) só conta um terço do nutriente que é encontrado no sal de cozinha.”
Dados de massas molares em g·mol-1 : sódio = 23, cloreto = 35,5, glutamato monossódico = 169.
Para tornar a argumentação do artigo mais consistente do ponto de vista químico, você sugeriria a seguinte reescrita dos trechos destacados:
Episódios recentes de erupções vulcânicas têm trazido
consequências trágicas para a sociedade e para o meio
ambiente. Ativo desde 1983, o Vulcão Kilauea apresentou,
em 2018, a sua maior erupção já registrada. Quase ao
mesmo tempo, foi a vez do Vulcão Fuego da Guatemala
mostrar sua força. No Kilauea não houve explosões, ao
contrário do que ocorreu no Fuego. Os especialistas
afirmam que a ocorrência de uma erupção explosiva
depende da concentração e do tipo de gases dissolvidos
no magma, como SO2, HF e HCl, além de vapor de água e
CO2 aprisionados. A figura a seguir dá informações sobre a
relação entre quantidades (em mol) de SO2, HF e HCl no
magma de três vulcões distintos.

De acordo com a figura, em relação às quantidades de
gases dissolvidos no magma, é correto afirmar que as
concentrações de SO2 são maiores que as de HF e de HCl

Dois estudantes, de massa corporal em torno de 75 kg, da
Universidade de Northumbria, no Reino Unido, quase
morreram ao participar de um experimento científico no
qual seriam submetidos a determinada dose de cafeína e a
um teste físico posterior. Por um erro técnico, ambos
receberam uma dose de cafeína 100 vezes maior que a
dose planejada. A dose planejada era de 0,3 g de cafeína,
equivalente a três xícaras de café. Sabe-se que a União
Europeia, onde o teste ocorreu, classifica a toxicidade de
uma dada substância conforme tabela a seguir.

Considerando que a DL50 – dose necessária de uma dada
substância para matar 50% de uma população – da cafeína
é de 192 mg/kg, no teste realizado a dose aplicada foi
cerca de

As empresas que fabricam produtos de limpeza têm se
preocupado cada vez mais com a satisfação do
consumidor e a preservação dos materiais que estão
sujeitos ao processo de limpeza. No caso do vestuário, é
muito comum encontrarmos a recomendação para fazer o
teste da firmeza das cores para garantir que a roupa não
será danificada no processo de lavagem. Esse teste
consiste em molhar uma pequena parte da roupa e colocá-
la sobre uma superfície plana; em seguida, coloca-se um
pano branco de algodão sobre sua superfície e passa-se
com um ferro bem quente. Se o pano branco ficar
manchado, sugere-se que essa roupa deve ser lavada
separadamente, pois durante esse teste ocorreu um
processo de
A comparação entre as proporções isotópicas de amostras
de um mesmo material, que têm a mesma idade,
encontradas em diferentes regiões, pode ser utilizada para
revelar se elas têm ou não a mesma origem. Se as
proporções são iguais, então é possível que tenham a
mesma origem, mas se forem diferentes, é certeza que não
têm a mesma origem. A tabela a seguir apresenta os dados
de algumas amostras de água, incluindo a de um cometa no
qual uma sonda pousou recentemente.

*nd – não disponível
Com base nesses dados, pode-se afirmar corretamente que
a água de nosso planeta
A comparação entre as proporções isotópicas de amostras de um mesmo material, que têm a mesma idade, encontradas em diferentes regiões, pode ser utilizada para revelar se elas têm ou não a mesma origem. Se as proporções são iguais, então é possível que tenham a mesma origem, mas se forem diferentes, é certeza que não têm a mesma origem. A tabela a seguir apresenta os dados de algumas amostras de água, incluindo a de um cometa no qual uma sonda pousou recentemente.

*nd – não disponível
Com base nesses dados, pode-se afirmar corretamente que
a água de nosso planeta
Alguns trabalhos científicos correlacionam as mudanças
nas concentrações dos sais dissolvidos na água do mar
com as mudanças climáticas. Entre os fatores que
poderiam alterar a concentração de sais na água do mar
podemos citar: evaporação e congelamento da água do
mar, chuva e neve, além do derretimento das geleiras. De
acordo com o conhecimento químico, podemos afirmar
corretamente que a concentração de sais na água do mar
O trecho seguinte foi extraído de uma revista de divulgação do
conhecimento químico, e trata de alguns aspectos da lavagem
a seco de tecidos. “Tratando-se do desempenho para lavar, o
tetracloroetileno é um solvente efetivo para limpeza das
roupas, pois evita o encolhimento dos tecidos, já que evapora
facilmente, dada sua baixa pressão de vapor (0,017 atm.,
20° C), e dissolve manchas lipofílicas, como óleos, ceras e
gorduras em geral...” A leitura desse trecho sugere que o
tetracloroetileno é um líquido apolar e sua alta volatilidade
se deve ao seu baixo valor de pressão de vapor. Levando
em conta o conhecimento químico, pode-se
Com a crescente crise mundial de dengue, as pesquisas
pela busca tanto de vacinas quanto de repelentes de
insetos têm se intensificado. Nesse contexto, os compostos
I e II abaixo representados têm propriedades muito
distintas: enquanto um deles tem caráter ácido e atrai os
insetos, o outro tem caráter básico e não os atrai.

Baseado nessas informações, pode-se afirmar
corretamente que o composto
Com a crescente crise mundial de dengue, as pesquisas pela busca tanto de vacinas quanto de repelentes de insetos têm se intensificado. Nesse contexto, os compostos I e II abaixo representados têm propriedades muito distintas: enquanto um deles tem caráter ácido e atrai os insetos, o outro tem caráter básico e não os atrai.

Baseado nessas informações, pode-se afirmar
corretamente que o composto
Hot pack e cold pack são dispositivos que permitem, respectivamente, aquecer ou resfriar objetos rapidamente e nas mais diversas situações. Esses dispositivos geralmente contêm substâncias que sofrem algum processo quando eles são acionados. Dois processos bastante utilizados nesses dispositivos e suas respectivas energias estão esquematizados nas equações 1 e 2 apresentadas a seguir.
NH4NO3(s)+H2O( l ) →NH4+(aq)+NO3-(aq) ΔΗ = 26 kJ mol-1 1
CaCl2(s)+H2O( l ) →Ca2+ (aq)+2Cl-(aq) ΔΗ = - 82 kJ mol-1 2
De acordo com a notação química, pode-se afirmar que as equações 1 e 2 representam processos de
NH4NO3(s)+H2O( l ) →NH4+(aq)+NO3-(aq) ΔΗ = 26 kJ mol-1 1
CaCl2(s)+H2O( l ) →Ca2+ (aq)+2Cl-(aq) ΔΗ = - 82 kJ mol-1 2
De acordo com a notação química, pode-se afirmar que as equações 1 e 2 representam processos de