TEXTO 4
Aprígio – Saia, Dália! (Dália abandona o quarto,
correndo, em desespero. Sogro e genro, face a face)
Vim aqui para.
Arandir (para o sogro quase chorando) – Está satisfeito?
Aprígio – Vim aqui.
Arandir (na sua cólera) – Está satisfeito? O senhor
é um dos responsáveis. Eu acho que é o senhor. O
senhor que está por trás...
Aprígio – Quem sabe?
Arandir – Por trás desse repórter. O senhor teve a
coragem de. Ou pensa que eu não sei? Selminha me
contou. Contou tudo! O senhor fez insinuações. Insinuações!
A meu respeito!
Aprígio – Você quer me.
Arandir (sem ouvi-lo) – O senhor fez tudo! Tudo pra
me separar de Selminha!
Aprígio – Posso falar?
Arandir (erguendo a voz) – O senhor não queria o
nosso casamento!
Aprígio (violento) – Escuta! Vim aqui saber! Escuta!
Você conhecia esse rapaz?
Arandir (desesperado) – Nunca vi.
Aprígio – Era um desconhecido?
Arandir – Juro! Por tudo que há de mais! Que nunca,
nunca!
Aprígio – Mentira!
Arandir (desesperado) – Vi pela primeira vez!
Aprígio – Cínico! (muda de tom, com uma Ferocidade)
Escuta! Você conhecia o rapaz. Conhecia! Eram
amantes! E você matou. Empurrou o rapaz!
Arandir (violento) – Deus sabe!
Aprígio – Eu não acredito em você. Ninguém acredita.
Os jornais, as rádios! Não há uma pessoa, uma
única, em toda a cidade. Ninguém!
Arandir (com a voz estrangulada) – Ninguém acredita,
mas eu! Eu acredito, acredito em mim!
Aprígio – Você, olha!
Arandir – Selminha há de acreditar!
Aprígio (fora de si) – Cala a boca! (muda de tom) Eu
te perdoaria tudo! Eu perdoaria o casamento. Escuta!
Ainda agora, eu estava na porta ouvindo. Ouvi tudo.
Você tentando seduzir a minha filha menor!
Arandir – Nunca!
Aprígio – Mas eu perdoaria, ainda. Eu perdoaria
que você fosse espiar o banho da cunhada. Você quis
ver a cunhada nua.
Arandir – Mentira!
Aprígio – Eu perdoaria tudo. (mais violento) Só não
perdoo o beijo no asfalto. Só não perdoo o beijo que
você deu na boca de um homem!
Arandir (para si mesmo) – Selminha!
Aprígio (muda de tom, suplicante) – Pela última vez, diz! Eu preciso saber! Quero a verdade! A verdade!
Vocês eram amantes? (sem esperar a resposta, furioso)
Mas não responda. Eu não acredito. Nunca, nunca,
eu acreditarei. (numa espécie de uivo) Ninguém
acredita!
Arandir – Vou buscar minha mulher. (Aprígio recua,
puxando o revólver.)
Aprígio (apontando) – Não se mexa! Fique onde
está!
Arandir (atônito) – O senhor vai.
Aprígio – Você era o único homem que não podia
casar com a minha filha! O único!
Arandir (atônito e quase sem voz) – O senhor me
odeia porque. Deseja a própria filha. É paixão. Carne.
Tem ciúmes de Selminha.
Aprígio (num berro) – De você! (estrangulando a voz)
Não de minha filha. Ciúmes de você. Tenho! Sempre.
Desde o teu namoro, que eu não digo o teu nome. Jurei
a mim mesmo que só diria teu nome a teu cadáver.
Quero que você morra sabendo. O meu ódio é amor.
Por que beijaste um homem na boca? Mas eu direi o
teu nome. Direi teu nome a teu cadáver.
(Aprígio atira, a primeira vez. Arandir cai de joelhos.
Na queda, puxa uma folha de jornal, que estava aberta
na cama. Torcendo-se. abre o jornal, como uma
espécie de escudo ou bandeira. Aprígio atira, novamente,
varando o papel impresso. Num espasmo de
dor, Arandir rasga a folha. E tomba, enrolando-se no
jornal. Assim morre.)
Aprígio – Arandir! (mais forte) Arandir! (um último
canto) Arandir!
Cai a luz, em resistência, sobre o cadáver de Arandir.
Trevas.
(RODRIGUES, Nelson. O beijo no asfalto. Rio
de Janeiro: Nova Fronteira, 1995. p. 101-104.)







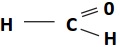 → BAQUELITE (FÓRMICA)
→ BAQUELITE (FÓRMICA)