Uma lagarta ao comer as folhas do milho, induz no
vegetal a produção de óleos voláteis cujas estruturas
estão mostradas a seguir:

A volatilidade desses óleos é decorrência do(a)


Os hidrocarbonetos são moléculas orgânicas com uma série de aplicações industriais. Por exemplo, eles estão presentes em grande quantidade nas diversas frações do petróleo e normalmente são separados por destilação fracionada, com base em suas temperaturas de ebulição. O quadro apresenta as principais frações obtidas na destilação do petróleo em diferentes faixas de temperaturas.

Na fração 4, a separação dos compostos ocorre em temperaturas mais elevadas porque

Um método para determinação do teor de etanol na gasolina consiste em misturar volumes conhecidos de água e de gasolina em um frasco específico. Após agitar o frasco e aguardar um período de tempo, medem-se os volumes das duas fases imiscíveis que são obtidas: uma orgânica e outra aquosa. O etanol, antes miscível com a gasolina, encontra-se agora miscível com a água.
Para explicar o comportamento do etanol antes e depois da adição de água, é necessário conhecer
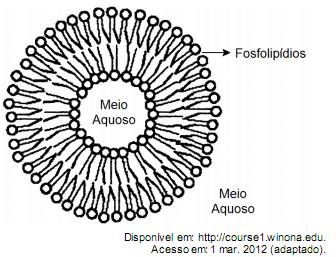
A fosfatidilserina é um fosfolipídio aniônico cuja interação com cálcio livre regula processos de transdução celular e vem sendo estudada no desenvolvimento de biossensores nanométricos. A figura representa a estrutura da fosfatidilserina:

Com base nas informações do texto, a natureza da interação da fosfatidilserina com o cálcio livre é do tipo
Dado: número atômico do elemento cálcio: 20
Sais de amônio são sólidos iônicos com alto ponto de fusão, muito mais solúveis em água que as aminas originais e ligeiramente solúveis em solventes orgânicos apolares, sendo compostos convenientes para serem usados em xaropes e medicamentos injetáveis. Um exemplo é a efedrina, que funde a 79 °C, tem um odor desagradável e oxida na presença do ar atmosférico formando produtos indesejáveis. O cloridrato de efedrina funde a 217 °C, não se oxida e é inodoro, sendo o ideal para compor os medicamentos.

De acordo com o texto, que propriedade química das aminas possibilita a formação de sais de amônio estáveis,
facilitando a manipulação de princípios ativos?
A absorção e o transporte de substâncias tóxicas em sistemas vivos dependem da facilidade com que estas se difundem através das membranas das células. Por apresentar propriedades químicas similares, testes laboratoriais empregam o octan-1-ol como modelo da atividade das membranas. A substância a ser testada é adicionada a uma mistura bifásica do octan-1-ol com água, que é agitada e, ao final, é medido o coeficiente de partição octan-1-ol:água (Koa):

em que Coct é a concentração da substância na fase do octan-1-ol, e Ca a concentração da substância na fase aquosa.
Foram avaliados cinco poluentes de sistemas aquáticos: benzeno, butano, éter dietílico, fluorobutano e metanol.
O poluente que apresentou Koa tendendo a zero é o
Os polímeros são materiais amplamente utilizados na sociedade moderna, alguns deles na fabricação de embalagens e filmes plásticos, por exemplo. Na figura estão relacionadas as estruturas de alguns monômeros usados na produção de polímeros de adição comuns.

Dentre os homopolímeros formados a partir dos monômeros da figura, aquele que apresenta solubilidade em água é
Os tensoativos são compostos capazes de interagir com substâncias polares e apolares. A parte iônica dos tensoativos interage com substâncias polares, e a parte lipofílica interage com as apolares. A estrutura orgânica de um tensoativo pode ser representada por:
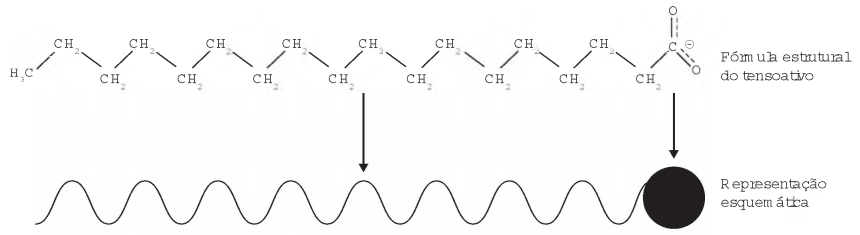
Ao adicionar um tensoativo sobre a água, suas moléculas formam um arranjo ordenado.
Esse arranjo é representado esquematicamente por:





A lipofilia é um dos fatores fundamentais para o planejamento de um fármaco. Ela mede o grau de afinidade que a substância tem com ambientes apolares, podendo ser avaliada por seu coeficiente de partição.
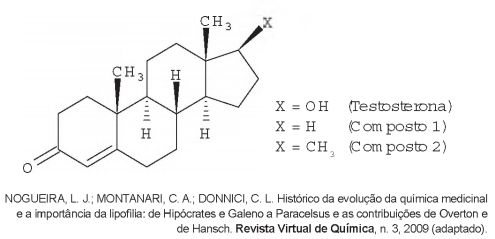
Em relação ao coeficiente de partição da testosterona, as
lipofilias dos compostos 1 e 2 são, respectivamente,