7bc9f1a8-e3
UEM 2013, UEM 2013, UEM 2013 - Química - Grandezas: massa, volume, mol, massa molar, constante de Avogadro e Estequiometria., Sistemas Gasosos - Lei, Teoria Cinética, Equação e Mistura dos Gases. Princípio de Avogadro., Transformações Químicas, Representação das transformações químicas
1 mol de H2O2 libera 11,2 L de O2.
1 mol de H2O2 libera 11,2 L de O2.
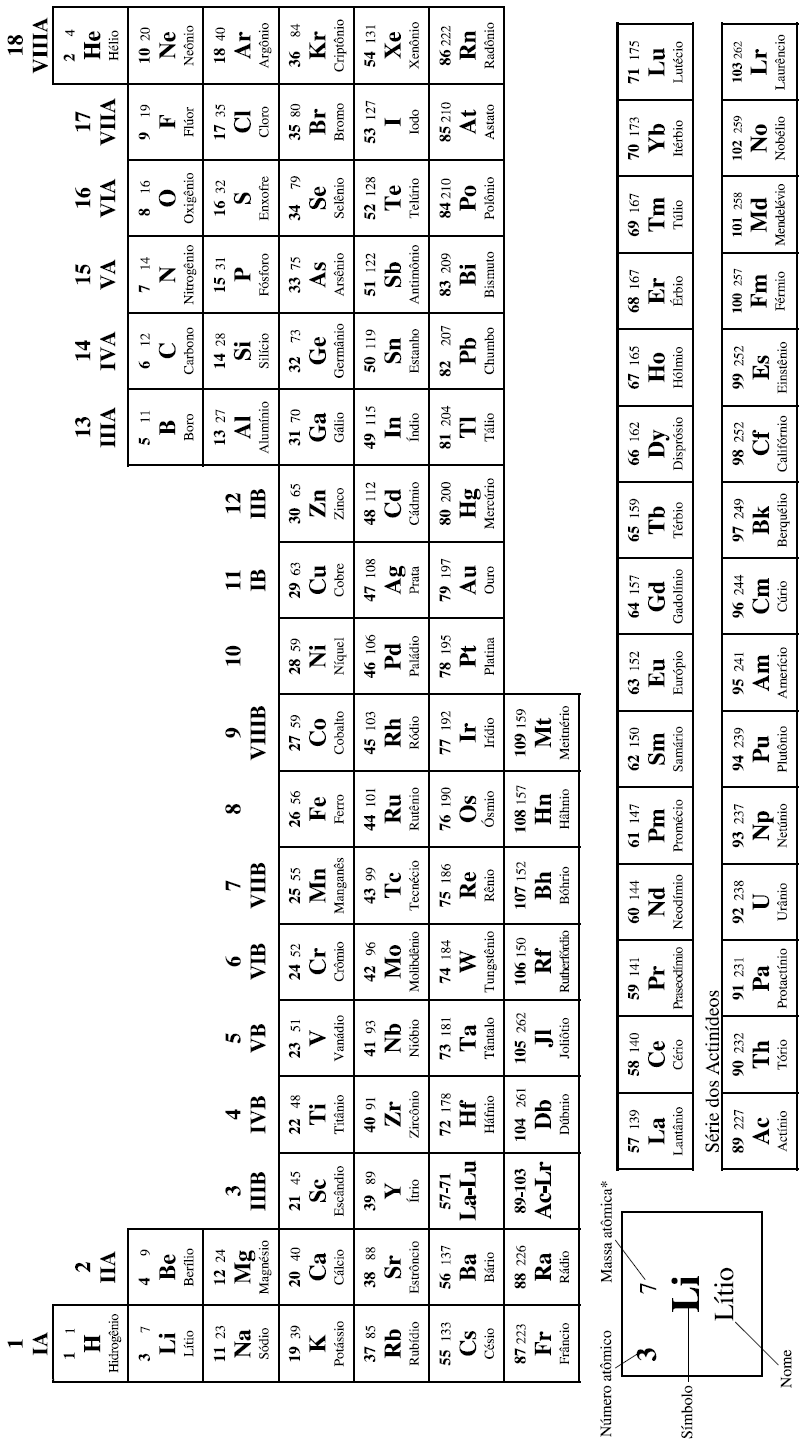
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADAS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE PROCESSO SELETIVO E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Em frascos de água oxigenada, a concentração dessa é expressa em volumes, como água oxigenada a 10 volumes, a 20 volumes etc. Essa concentração corresponde ao número de litros de gás oxigênio medido nas condições normais de temperatura e pressão (CNTP), obtidos pela decomposição completa de todo H2O2 em um litro de solução. Considerando que a reação abaixo transcorra na CNTP e que R = 0,082 atm.L.mol-1K-1, assinale o que for correto.
1 H2O(l)  1 H2O(l) + 1/2 O2(g)
1 H2O(l) + 1/2 O2(g)
 1 H2O(l) + 1/2 O2(g)
1 H2O(l) + 1/2 O2(g)
C
Certo
E
Errado