Questõessobre Grandezas: massa, volume, mol, massa molar, constante de Avogadro e Estequiometria.
Uma solução apresenta uma concentração mássica de 30%
de um soluto e possui uma quantidade de solvente igual a 56 g. A massa
dessa solução é igual a:
Suponha que uma indústria possua 5 000 kg de calcário
com 90% de pureza em CaCO3 e quer obter CaO (cal virgem) por
decomposição térmica desse material. Que massa de cal virgem será obtida
no processo se este apresentar 80% de rendimento?
Dados massas molares: Ca = 40; C = 12; O = 16
CaCO3  CaO + CO2
CaO + CO2
 CaO + CO2
CaO + CO2Vem de uma flor, cura a dor, mas causa
morte e pavor. É a aspirina, o remédio mais
conhecido do mundo. Contém o ácido acetilsalicílico
existente em flores do gênero Spirae, muito usadas
em buquês de noivas. Além de curar a dor, esse
ácido também é usado para proteger o coração de
doenças, pois ele também impede a formação de
coágulos, mas, se usado indiscriminadamente, pode
causar a morte. Veja a estrutura de uma molécula
desse ácido e assinale a afirmação verdadeira.


DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
O conhecimento dos conceitos de oxidação e
redução é de fundamental importância no estudo da
biologia molecular associado à fotossíntese e à
respiração, na redução de minerais para a obtenção
de metais, em cálculos estequiométricos, na
prevenção da corrosão e no estudo da
eletroquímica. Dada a equação não balanceada,
As2S3 +HNO3 + H2O → H3AsO4 + H2SO4 +NO,
marque a única afirmação verdadeira.
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
Existem diversos tipos de água mineral e sua classificação está relacionada à fonte em que
são captadas. Nela estão presentes vários sais dissolvidos. Baseando-se na composição
química informada na tabela 1 a seguir, a quantidade de mols de cálcio presente em um
recipiente com 500 mL de água mineral é:
Tabela 1: Composição química de uma água mineral
Composição química mg/L
Bicarbonato 82,7 Cálcio 16,0
Cloreto 1,1 Fluoreto 0,1 Magnésio 0,2 Potássio 0,3 Sódio 15,2
O vidro é um sólido iônico que tem a estrutura amorfa
lembrando a de um líquido. Os vidros têm estrutura em
rede baseada nos óxidos não-metálicos, normalmente
a sílica, SiO2, fundida juntamente com óxidos
metálicos que agem como “modificadores de rede”. O
vidro é resistente ao ataque da maioria dos reagentes.
Entretanto, a sílica do vidro reage com íons fluoreto
para formar íons fluorossilicatos, como mostrado na
equação:
SiO2(s) + 6 HF(aq) → SiF62−(aq) + 2 H3O+
(aq)
Calcule a massa de ácido fluorídrico necessária para
reagir com 1,0 kg de SiO2.
Dados: Massas molares em g . mol-1
: H = 1; F = 19;
O = 16; Si = 28.
Calcule a massa de ácido fluorídrico necessária para reagir com 1,0 kg de SiO2.
Dados: Massas molares em g . mol-1 : H = 1; F = 19; O = 16; Si = 28.
O iodeto de potássio (KI) é um sólido branco que pode
ser utilizado na formulação de xaropes mucolíticos e
expectorantes.
A porcentagem, em massa, de iodo na unidade formal de
iodeto de potássio é



Bicarbonato de sódio é uma substância de múltiplas
utilidades, entre elas: é um antiácido; é usado por dentistas para limpeza dos dentes e por cozinheiros para acelerar a cocção de vários alimentos.
Sua fórmula é NaHCO3
Um estudante, que gosta de fazer graça com os outros,foi a uma farmácia e pediu 1 mol de bicarbonato de sódio.
O farmacêutico, que sabia bastante química (obviamente), informou ao estudante que tinha uma embalagem de 80 gramas e que esta quantidade teria,aproximadamente, 1 mol de bicarbonato de sódio.
Na verdade, podemos afirmar que

Bicarbonato de sódio é uma substância de múltiplas
utilidades, entre elas: é um antiácido; é usado por dentistas para limpeza dos dentes e por cozinheiros para acelerar a cocção de vários alimentos.
Sua fórmula é NaHCO3
Um estudante, que gosta de fazer graça com os outros,foi a uma farmácia e pediu 1 mol de bicarbonato de sódio.
O farmacêutico, que sabia bastante química (obviamente), informou ao estudante que tinha uma embalagem de 80 gramas e que esta quantidade teria,aproximadamente, 1 mol de bicarbonato de sódio.
Na verdade, podemos afirmar que

Uma motocicleta pequena
apresenta um tanque de combustível que
pode armazenar 10 litros. Sabemos que a
gasolina distribuída para a população, a
chamada gasolina vermelha, apresenta
teor de álcool igual a 25%. Se um
motociclista vai percorrer uma distância
que irá gastar metade do combustível de
seu tanque, a massa de álcool que irá
queimar nesse percurso é igual a:
(Dado: Etanol → d = 0,80g / mL)
O dióxido de enxofre (SO2), produto da combustão do
carvão em centrais termoelétricas, é o mais importante
precursor da chuva ácida, ocasionando impacto nas
florestas, pastos, lavouras, ambientes aquáticos e
afetando o solo. Uma tecnologia de dessulfurização
de gás de chaminé, para limitar a emissão de SO2,
utiliza o CaCO3
como adsorvente deste gás e gera o
gesso (sulfato de cálcio). Segundo dados do IPCC2006 (Intergovernmental Panel on Climate Change),
no mundo, aproximadamente 1012 g de SO2
deixam de
ser emitidos por ano devido à utilização de tecnologias
de dessulfurização dos gases de exaustão após combustão do carvão. Considerando que toda tecnologia de
dessulfurização empregue carbonato de cálcio, a massa
de gesso produzida em um ano, a partir do consumo
de 1012 g de SO2
, com rendimento de 100%, de acordo
com a equação química a seguir, é de aproximadamente
2 CaCO3(s) + 2 SO2(g) + O2(g) → 2 CaSO4(g) + 2 CO2(g)
O dióxido de enxofre (SO2), produto da combustão do carvão em centrais termoelétricas, é o mais importante precursor da chuva ácida, ocasionando impacto nas florestas, pastos, lavouras, ambientes aquáticos e afetando o solo. Uma tecnologia de dessulfurização de gás de chaminé, para limitar a emissão de SO2, utiliza o CaCO3 como adsorvente deste gás e gera o gesso (sulfato de cálcio). Segundo dados do IPCC2006 (Intergovernmental Panel on Climate Change), no mundo, aproximadamente 1012 g de SO2 deixam de ser emitidos por ano devido à utilização de tecnologias de dessulfurização dos gases de exaustão após combustão do carvão. Considerando que toda tecnologia de dessulfurização empregue carbonato de cálcio, a massa de gesso produzida em um ano, a partir do consumo de 1012 g de SO2 , com rendimento de 100%, de acordo com a equação química a seguir, é de aproximadamente
2 CaCO3(s) + 2 SO2(g) + O2(g) → 2 CaSO4(g) + 2 CO2(g)
INSTRUÇÃO: Para responder à questão, analise a representação do glifosato a seguir.

O uso de agrotóxicos é objeto de preocupações, pois o contato com doses elevadas no momento da aplicação tem causado sérios problemas de saúde a trabalhadores rurais. Esse problema se agrava quando os agricultores aplicam doses maiores do que as recomendadas, em uma tentativa de controlar pragas resistentes. O glifosato, por exemplo, no uso agrícola comum, é adquirido como uma solução com a concentração de 360 gramas por litro, sendo aplicados cinco litros por hectare (um hectare equivale a 10000 m²).
Sobre esse assunto, fazem-se as seguintes afirmativas.
I. Em uma aplicação de glifosato, cada hectare de lavoura recebe mais de 1,0×1023 moléculas desse herbicida.
II. Em uma molécula de glifosato há mais átomos de hidrogênio do que de oxigênio.
III. A concentração de glifosato na solução é de aproximadamente 2,1 mol/L.
Está/Estão correta(s) a(s) afirmativa(s)
INSTRUÇÃO: Para responder à questão, analise a representação do glifosato a seguir.

O uso de agrotóxicos é objeto de preocupações, pois o contato com doses elevadas no momento da aplicação tem causado sérios problemas de saúde a trabalhadores rurais. Esse problema se agrava quando os agricultores aplicam doses maiores do que as recomendadas, em uma tentativa de controlar pragas resistentes. O glifosato, por exemplo, no uso agrícola comum, é adquirido como uma solução com a concentração de 360 gramas por litro, sendo aplicados cinco litros por hectare (um hectare equivale a 10000 m²).
Sobre esse assunto, fazem-se as seguintes afirmativas.
I. Em uma aplicação de glifosato, cada hectare de lavoura recebe mais de 1,0×1023 moléculas desse herbicida.
II. Em uma molécula de glifosato há mais átomos de hidrogênio do que de oxigênio.
III. A concentração de glifosato na solução é de aproximadamente 2,1 mol/L.
Está/Estão correta(s) a(s) afirmativa(s)
I, II e III.
O airbag (“bolsa de ar”) é um equipamento de segurança obrigatório em muitos países que já
ajudou a salvar muitas vidas em acidentes de carro. Segundo um levantamento feito pelo Instituto de Segurança do Trânsito dos Estados Unidos, desde que o airbag se tornou obrigatório, no ano de 1995, até o ano de
2007, ele ajudou a salvar mais de 15 mil pessoas. Essas bolsas são feitas de um material bastante reforçado,
que costuma ser o polímero náilon, que é bem resistente. No interior dessa bolsa, há uma mistura de reagentes: azoteto de sódio (NaN3), nitrato de potássio e dióxido de silício. No momento da colisão, sensores localizados em pontos estratégicos do carro detectam a forte desaceleração do veículo e são acionados, emitindo sinais para uma unidade de controle, que checa qual sensor foi atingido e, assim, aciona o airbag mais
adequado. O sensor é ligado a um filamento que fica em contato com uma pastilha de azoteto de sódio dentro
do airbag. Ele emite então uma faísca ou descarga elétrica, que aquece o azoteto, fornecendo a energia de
ativação necessária para dar início à reação demonstrada a seguir, que libera grande quantidade de gás
nitrogênio (N2).
Disponível em: <http://alunosonline.uol.com.br/>
NaN3 (s) → Na(s) + N2(g)
Analisando o texto, assinale a alternativa CORRETA.
A redução de grandes quantidades de dióxido de silício é
um processo industrial importante descrito pela equação
química abaixo.
SiO2(s) + C(s) → Si(s) + CO2(g)
Considerando a reação completa, a massa de silício, em
gramas, formada pela reação de 24.000 g de SiO2
com
excesso de carbono é










A hidrazina (N2H4) é usada como combustível
para foguetes e pode ser obtida a partir da
reação entre cloramina e amônia,
apresentada abaixo.
NH2Cl + NH3 → N2H4 + HCl
Assinale a alternativa que apresenta a massa
de hidrazina que pode ser obtida pela reação
de 10,0 g de cloramina com 10,0 g de
amônia.
Por questões econômicas, a medalha de ouro não é 100% de ouro desde os jogos de 1912 em
Estocolmo, e sua composição varia nas diferentes edições dos jogos olímpicos. Para os jogos
olímpicos de 2016, no Rio de Janeiro, a composição das medalhas foi distribuída como apresenta o
quadro abaixo.

Considerando que as três medalhas tenham a mesma massa, assinale a alternativa que apresenta as
medalhas em ordem crescente de número de átomos metálicos na sua composição.

As nanopartículas de prata, usadas em diversas aplicações tecnológicas, podem ser preparadas, em solução
aquosa, pela redução de íons Ag+ usando boro-hidreto de sódio (NaBH4), como indicado na equação abaixo:
AgNO3 (aq) + NaBH4 (aq) → Ag (s) + ½ H2 (g) + ½ B2H6 (g) + NaNO3 (aq)
A partir de 100,00 mL de uma solução 2,0 × 10-3 mol L-1 de AgNO3, qual seria a massa mínima de NaBH4
necessária para a reação completa de Ag+ para Ag, expressa em gramas?
Dados:
M(AgNO3) = 170 g mol-1
M(Ag) = 108 g mol-1
M(NaBH4) = 38 g mol-1
As nanopartículas de prata, usadas em diversas aplicações tecnológicas, podem ser preparadas, em solução aquosa, pela redução de íons Ag+ usando boro-hidreto de sódio (NaBH4), como indicado na equação abaixo:
AgNO3 (aq) + NaBH4 (aq) → Ag (s) + ½ H2 (g) + ½ B2H6 (g) + NaNO3 (aq)
A partir de 100,00 mL de uma solução 2,0 × 10-3 mol L-1 de AgNO3, qual seria a massa mínima de NaBH4 necessária para a reação completa de Ag+ para Ag, expressa em gramas?
Dados:
M(AgNO3) = 170 g mol-1
M(Ag) = 108 g mol-1
M(NaBH4) = 38 g mol-1
Um comprimido efervescente de vitamina C contém
500 mg de ácido ascórbico (C6H8O6
). Quando um paciente bebe água em que foram dissolvidos dois comprimidos
de vitamina C, ele consumiu um número mais próximo de
moléculas de ácido ascórbico de
Dados
MC6H8O6= 176 g mol-1
N° Avogadro = 6 x 1023 moléculas . mol-1
Um comprimido efervescente de vitamina C contém 500 mg de ácido ascórbico (C6H8O6 ). Quando um paciente bebe água em que foram dissolvidos dois comprimidos de vitamina C, ele consumiu um número mais próximo de moléculas de ácido ascórbico de
Dados
MC6H8O6= 176 g mol-1
N° Avogadro = 6 x 1023 moléculas . mol-1
A redução de grandes quantidades de dióxido de silício é
um processo industrial importante descrito pela equação
química abaixo.
SiO2(s) + C(s) → Si(s) + CO2(g)
Considerando a reação completa, a massa de silício, em
gramas, formada pela reação de 24.000 g de SiO2
com
excesso de carbono é
Dados
M(Si): 28 g mol-1
M(O): 16 g mol-1
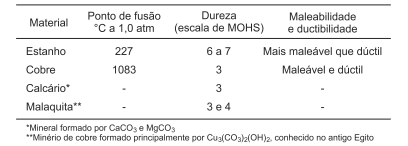
Com base nos conhecimentos de Química e nas propriedades físicas de alguns materiais utilizados na construção da Pirâmide
de Quéops, no Egito, por volta de 2525 a.C., é correto concluir:
