O TBT (M.M = 291 g/mol) é um composto polar,
hidrofóbico e lipofílico que foi introduzido no mercado nos
anos 40. É componente de tintas anti-incrustantes, utilizadas em cascos de barcos, redes e jaulas de aquacultura a
fim de impedir a fixação de organismos como algas e invertebrados (mexilhão, cracas, etc.). Além disso, o TBT é utilizado também na agricultura como pesticida, conservante
de madeiras e, numa escala menor, em desinfetantes e em
tratamentos algicidas em materiais de construção. A sua
elevada difusão no meio marinho tornou-se uma preocupação ambiental em nível mundial. Atualmente, é considerada
a substância mais tóxica produzida pelo homem.
A composição centesimal do TBT é de 49.49% de Carbono,
9.62% de Hidrogênio e 40.89% de Estanho e sua fórmula
molecular é:
O TBT (M.M = 291 g/mol) é um composto polar, hidrofóbico e lipofílico que foi introduzido no mercado nos anos 40. É componente de tintas anti-incrustantes, utilizadas em cascos de barcos, redes e jaulas de aquacultura a fim de impedir a fixação de organismos como algas e invertebrados (mexilhão, cracas, etc.). Além disso, o TBT é utilizado também na agricultura como pesticida, conservante de madeiras e, numa escala menor, em desinfetantes e em tratamentos algicidas em materiais de construção. A sua elevada difusão no meio marinho tornou-se uma preocupação ambiental em nível mundial. Atualmente, é considerada a substância mais tóxica produzida pelo homem.
A composição centesimal do TBT é de 49.49% de Carbono, 9.62% de Hidrogênio e 40.89% de Estanho e sua fórmula molecular é:
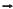 Al 2 O3(s) , não balanceada, pode-se afirmar que a massa de alumínio necessária para produzir 51 g de óxido de alumínio é
Al 2 O3(s) , não balanceada, pode-se afirmar que a massa de alumínio necessária para produzir 51 g de óxido de alumínio é