Questõessobre Estrutura Atômica: números de massa, átomo neutro e íon, elemento químico e semelhanças atômicas
Sabendo que um átomo possui 12 prótons, 13 nêutrons e 12 elétrons, pode-se afirmar que:
A eletroafinidade do átomo de potássio é maior que a do átomo de cloro.

O teste de chamas é um experimento realizado principalmente ao se estudar o conceito do modelo atômico de Rutherford-Böhr.
Com base nos conhecimentos sobre estrutura atômica e propriedades periódicas, é correto afirmar:
O raio atômico do flúor é maior que o do lítio.

O teste de chamas é um experimento realizado principalmente ao se estudar o conceito do modelo atômico de Rutherford-Böhr.
Com base nos conhecimentos sobre estrutura atômica e propriedades periódicas, é correto afirmar:
Os raios iônicos variam da sequência Na+> Mg2+> Al3+.

O teste de chamas é um experimento realizado principalmente ao se estudar o conceito do modelo atômico de Rutherford-Böhr.
Com base nos conhecimentos sobre estrutura atômica e propriedades periódicas, é correto afirmar:
A distribuição eletrônica do átomo do tungstênio apresenta elétrons mais energéticos no subnível 5d e
elétrons mais externos no subnível 6s.

O teste de chamas é um experimento realizado principalmente ao se estudar o conceito do modelo atômico de Rutherford-Böhr.
Com base nos conhecimentos sobre estrutura atômica e propriedades periódicas, é correto afirmar:
Isótopos são átomos com o mesmo número de massa.

O teste de chamas é um experimento realizado principalmente ao se estudar o conceito do modelo atômico de Rutherford-Böhr.
Com base nos conhecimentos sobre estrutura atômica e propriedades periódicas, é correto afirmar:
A carga nuclear efetiva Zef experimentada pelo elétron é sempre maior que a carga nuclear nominal.

O teste de chamas é um experimento realizado principalmente ao se estudar o conceito do modelo atômico de Rutherford-Böhr.
Com base nos conhecimentos sobre estrutura atômica e propriedades periódicas, é correto afirmar:
Em 2014, na Alemanha, um elemento pesado foi
confirmado por experimentos com um colisor
de partículas e ocupará sua justa posição como
Elemento 117 na Tabela Periódica.
Bombardeando amostras de berquélio radioativo
com átomos de cálcio, pesquisadores criaram
átomos com 117 prótons, originando um elemento
químico, aproximadamente, 42% mais pesado que
o chumbo e com meia-vida relativamente longa.
Os físicos apelidaram, temporariamente, o novo
integrante da Tabela Periódica como “ununséptio”
(Uus), alusão direta ao numeral 117, que é a soma
dos 20 prótons do cálcio com os 97 do berquélio.
(http://tinyurl.com/m8nlkq2 Acesso em: 13.06.2014. Adaptado)
De acordo com o texto, a massa atômica aproximada do
ununséptio é

Em 2014, na Alemanha, um elemento pesado foi confirmado por experimentos com um colisor de partículas e ocupará sua justa posição como Elemento 117 na Tabela Periódica.
Bombardeando amostras de berquélio radioativo com átomos de cálcio, pesquisadores criaram átomos com 117 prótons, originando um elemento químico, aproximadamente, 42% mais pesado que o chumbo e com meia-vida relativamente longa. Os físicos apelidaram, temporariamente, o novo integrante da Tabela Periódica como “ununséptio” (Uus), alusão direta ao numeral 117, que é a soma dos 20 prótons do cálcio com os 97 do berquélio.
(http://tinyurl.com/m8nlkq2 Acesso em: 13.06.2014. Adaptado)
De acordo com o texto, a massa atômica aproximada do ununséptio é

Analise as proposições seguintes e assinale a única
alternativa correta:

Os íons cádmio,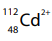 , presentes na água contaminada apresentam
, presentes na água contaminada apresentam
Os íons cádmio,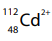 , presentes na água contaminada apresentam
, presentes na água contaminada apresentam
Leia o texto e a tabela para responder à questão.
Barcarena, no nordeste do Pará, é uma cidade da Amazônia marcada por desastres ambientais. Há semanas, depois de fortes chuvas, houve um vazamento de rejeitos em uma das empresas do polo industrial, o que contaminou rios da região. No município de Barcarena já houve outros registros de crimes ambientais de contaminação.
Em 2004, a Universidade Federal do Pará (UFPA) realizou uma pesquisa que concluiu que a água consumida pela população, em 26 localidades, estava contaminada por íons de metais pesados tais como Pb2+, Cd2+ e Hg2+, descartados pelas indústrias. Amostras de água de Vila Nova, Burajuba e do Distrito Industrial apresentaram concentração de chumbo 12 vezes maior que o máximo permitido por uma resolução de 2011 do Ministério da Saúde.

Um átomo neutro X possui a seguinte distribuição eletrônica:
X ➔ 1s² 2s² 2p6 3s² 3p4
Sobre as propriedades químicas deste átomo, assinale a alternativa correta:
Um cátion bivalente de um determinado átomo possui 25 elétrons e 28 nêutrons. Qual é o
número atômico e o número de massa deste átomo, respectivamente?
Os íons Ca+2 e Pb+2 possuem(Dados: Número atômico: Ca = 20 ; Pb = 82)
O radônio, símbolo Rn, pertencente à família dos gases
nobres, encontrado no grupo 18 ou 8A da tabela periódica
dos elementos, é usado na radioterapia e na composição
de cápsulas para aplicação em pacientes com câncer.
Certo isótopo desse elemento possui 86 prótons,
86 elétrons e número de massa 222, logo o número de
nêutrons desse isótopo é
O mercúrio torna-se mais problemático para o ambiente quando, por meio de transformações químicas, forma o metilmercúrio, um cátion organometálico, representado por CH3Hg+. O
número total de elétrons presente nos átomos que constituem
esse cátion é
O urânio  é um elemento químico radioativo utilizado na construção da bomba atômica lançada na cidade
de Hiroshima, no Japão, durante a Segunda Guerra Mundial. O átomo de urânio apresenta:
é um elemento químico radioativo utilizado na construção da bomba atômica lançada na cidade
de Hiroshima, no Japão, durante a Segunda Guerra Mundial. O átomo de urânio apresenta:
O urânio  é um elemento químico radioativo utilizado na construção da bomba atômica lançada na cidade
de Hiroshima, no Japão, durante a Segunda Guerra Mundial. O átomo de urânio apresenta:
é um elemento químico radioativo utilizado na construção da bomba atômica lançada na cidade
de Hiroshima, no Japão, durante a Segunda Guerra Mundial. O átomo de urânio apresenta:
O iodo-131 é utilizado na terapia para o câncer. Dos nuclídeos indicados abaixo, o que é um isótono do 131I é o
Os valores de Z (N° Atômico), A (N° de Massa),
p+ (Prótons), e-
(Elétrons) e n° (Nêutrons) do íon
Potássio (K) carregado positivamente, na forma
catiônica, e com carga elétrica igual a +1, são respectivamente:
Dados: No estado fundamental o Potássio
(K) possui N° Atômico = 19 e N° de Massa = 39
Os valores de Z (N° Atômico), A (N° de Massa), p+ (Prótons), e- (Elétrons) e n° (Nêutrons) do íon Potássio (K) carregado positivamente, na forma catiônica, e com carga elétrica igual a +1, são respectivamente:
Dados: No estado fundamental o Potássio (K) possui N° Atômico = 19 e N° de Massa = 39
Áreas como a medicina, a agricultura e a indústria farmacêutica são beneficiadas com o desenvolvimento dos
estudos da radioatividade. A radioterapia – técnica utilizada para destruir células cancerosas – faz uso, principalmente, de
radioisótopos do iodo-131 para eliminar lesões identificadas nos radiodiagnósticos da tireoide.
Sobre esse radioisótopo, assinale a alternativa correta.
Áreas como a medicina, a agricultura e a indústria farmacêutica são beneficiadas com o desenvolvimento dos estudos da radioatividade. A radioterapia – técnica utilizada para destruir células cancerosas – faz uso, principalmente, de radioisótopos do iodo-131 para eliminar lesões identificadas nos radiodiagnósticos da tireoide.
Sobre esse radioisótopo, assinale a alternativa correta.