Questõessobre Estrutura Atômica: números de massa, átomo neutro e íon, elemento químico e semelhanças atômicas
Analisando o elemento genérico 15X32, pode-se
dizer que ele é isótopo do fósforo.

Alimentos como ovos, leite, manteiga e cacau fornecem ao organismo uma substância chamada ergosterol. Na presença de raios solares, nosso organismo transforma ergosterol em vitamina D. Essa vitamina favorece a retenção de Cálcio e de Fósforo nos ossos e nos dentes (REIS, Martha. Completamente Química: Vol. 1. São Paulo: FTD, 2001. p. 390). Dado que a massa molar do ergosterol e da vitamina D (calciferol) são 396,6 g mol–1 e 384,6 g mol–1, respectivamente, assinale o que for correto.
Indique qual propriedade periódica é representada pela
figura abaixo.
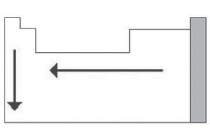
Indique qual propriedade periódica é representada pela figura abaixo.

O átomo Q tem 36 nêutrons e é isóbaro do átomo R.
Considerando que R+2 é isoeletrônico do átomo Q,
identifique o número de nêutrons do átomo R.
Se um elétron se move de um nível de energia de um
átomo para outro nível de energia mais afastado do
núcleo do mesmo átomo, pode-se afirmar que
Segundo dados experimentais, o oxigênio do ar que
respiramos contém exatos 99,759% de 8O16, 0,037%
de átomos de 8O17 e 0,204% de átomos de 8O18.
Diante desta constatação, pode-se afirmar que essas
três formas naturais de oxigênio constituem átomos que,
entre si, são
A energia gerada pelas usinas de energia
nuclear é produzida pela fissão nuclear. O
combustível nuclear deve ser uma substância de
natureza físsil como o 235U. Na natureza, o
urânio é encontrado na composição de 99,284%
do isótopo 238U e 0,711% do isótopo 235U. Para
ser usado como combustível nuclear, o urânio é
submetido a um processo de enriquecimento, a
fim de concentrar na mistura de isótopos o teor
do isótopo físsil. Com relação aos isótopos 235U
e 238U, é incorreto afirmar que os mesmos
possuem:
Atualmente a prescrição de carbonato de lítio, Li2CO3, tem sido
a forma mais segura para o tratamento de alguns tipos de
doença mental. Aparentemente, o lítio interfere, na forma iônica,
em mecanismos bioquímicos nos quais os íons magnésio, Mg2+,
estariam envolvidos, mas a sua função específica no cérebro
ainda é desconhecida.
Considerando-se essas informações, é correto afirmar:
Atualmente a prescrição de carbonato de lítio, Li2CO3, tem sido a forma mais segura para o tratamento de alguns tipos de doença mental. Aparentemente, o lítio interfere, na forma iônica, em mecanismos bioquímicos nos quais os íons magnésio, Mg2+, estariam envolvidos, mas a sua função específica no cérebro ainda é desconhecida.
Considerando-se essas informações, é correto afirmar:
Assinale o que for correto.
Quanto maior a diferença na eletronegatividade entre
os átomos participantes de uma ligação, maior a
probabilidade dessa ligação ser do tipo iônica.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Assinale o que for correto.
O potencial de ionização de um elemento cujo elétron
ionizável está em um subnível 3s é maior do que o
potencial de ionização de um elemento cujo elétron
ionizável está em um subnível 2s.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Assinale o que for correto.
O átomo de carbono possui 2 elétrons
desemparelhados em um orbital do tipo p.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Assinale o que for correto.
Um íon de carga 2+ que apresenta a distribuição
eletrônica 1s2
2s2
2p6
3s2
3p4
possui 18 prótons em
seu núcleo.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Leia o texto abaixo.

Pivetta Marcos. Traquinagens etílicas. Revista Pesquisa FAPESP Dez 2003. [Adaptado]
O teste descrito no texto se baseia na propriedade dos átomos de carbono conhecida como
Leia o texto abaixo.

Pivetta Marcos. Traquinagens etílicas. Revista Pesquisa FAPESP Dez 2003. [Adaptado]
O teste descrito no texto se baseia na propriedade dos átomos de carbono conhecida como

Os íons Mg2+ e F−
são isoeletrônicos, entretanto o raio iônico
do ânion fluoreto, F−
, é o dobro do raio do cátion magnésio,
Mg2+. Esses íons são constituídos no processo de doação e
de recebimento de elétrons durante a formação de ligação
iônica.
Uma análise dessas informações e da tabela, tendo como
base as propriedades periódicas dos elementos químicos,
permite afirmar:

Os íons Mg2+ e F− são isoeletrônicos, entretanto o raio iônico do ânion fluoreto, F− , é o dobro do raio do cátion magnésio, Mg2+. Esses íons são constituídos no processo de doação e de recebimento de elétrons durante a formação de ligação iônica.
Uma análise dessas informações e da tabela, tendo como
base as propriedades periódicas dos elementos químicos,
permite afirmar:
“...aquela substância esverdeada que se forma em volta da gema. Ela surge quando o sulfeto de hidrogênio presente na clara esquenta se expande .” Com relação ao sulfeto de hidrogênio, é correto
afirmar que
Nenhum lugar da casa se parece tanto com um laboratório de química quanto a cozinha, onde diversos ingredientes são misturados, queimados, fermentados e submetidos a processos dignos de experiências científicas. Assim como no laboratório, ter noções de química é essencial para que o cozinheiro consiga preparar corretamente os pratos, até os mais simples. Veja, por exemplo, como levar à perfeição a arte de cozinhar ovos.
Considerando a molécula de hidróxido de sódio e utilizando o fundamento da Lei
de Avogadro sobre as quantidades de moles contidos em substâncias, podemos
afirmar que, em 20 gramas de NaOH, temos:
O átomo de carbono é um elemento químico que se liga a ele mesmo formando alótropos (Figura 1)
ou às mais variadas cadeias carbônicas nos compostos orgânicos. O mais recente alótropo de
carbono é o Grafeno (Fig. 1f), que foi isolado e caracterizado em 2004, rendendo o prêmio Nobel de
Física de 2010 a seus autores, A. Geim e K. Novoselov, da Universidade de Manchester. A aplicação
potencial do Grafeno irá provocar uma revolução em breve no setor elétrico e eletrônico. Por isso,
vários cientistas no mundo e no Brasil pesquisam exaustivamente estes novos materiais.

Com relação a este assunto, são feitas as seguintes afirmações.
I - O átomo de Carbono-12 possui em seu núcleo seis nêutrons e seis prótons.
II - A descoberta do C60 (Fig. 1c), que tem a forma de uma bola de futebol, impulsionou a descoberta
de outras estruturas de fulerenos, principalmente materiais nanoestruturados, como os nanotubos
de carbono. Estas substâncias simples possuem uma massa molar de 720 g/mol.
III - O átomo de carbono tem seis elétrons na sua eletrosfera, por isso, é chamado de hexavalente.
Sendo assim, precisa apenas mais dois elétrons na sua camada de valência (camada mais
externa) para obedecer à regra do octeto.
IV - Numa combustão completa, as moléculas orgânicas presentes nos combustíveis fósseis se ligam
completamente ao gás oxigênio formando gás carbônico, que é um dos grandes responsáveis
pelo efeito estufa.
V - Quanto à disposição dos átomos de carbono na cadeia carbônica das moléculas orgânicas,
podemos classificá-las em Cadeia Normal (Reta ou Linear) ou Cadeia Ramificada.
Assinale a alternativa correta.

Assinale a alternativa correta.
A percepção visual da cor de uma solução depende da absorção da radiação. Dessa forma, uma solução é
magenta porque absorve o verde da luz branca que penetra no recipiente e transmite o magenta como cor
complementar no espectro. A Tabela 1 mostra a relação entre diferentes cores e a Tabela 2 mostra as
cores absorvidas por diferentes soluções contendo íons metálicos.

Na dissolução de três compostos metálicos foram visualizadas as seguintes colorações:
Sistema 1 - Violeta Sistema 2 - Ciano Sistema 3 - Laranja
Os íons presentes no sistema 1, 2 e 3 são, respectivamente:

A figura abaixo representa a TEOBROMINA, presente nos grãos de cacau e responsável pela ação
estimulante e energética do chocolate.

Fonte: DOSSIÊ CHOCOLATE: GRANDE VILÃO, UM INCOMPREENDIDO OU APENAS UM BOM ALIADO DA SAÚDE? Disponível em: http://www.jornalciencia.com/saude/beleza/2442-dossie-chocolate-grande-vilao-um-inc
Assinale a alternativa correta sobre a fórmula molecular da TEOBROMINA.
