114ac4c1-f5
UFRN 2012 - Química - Equilíbrio Químico, Sistemas Homogêneos: Equilíbrio Químico na Água: pH e pOH, Indicadores Ácido-Base, Solução Tampão.
O pH é um dos parâmetros da qualidade da água doce para consumo. Os valo res dos parâmetros
da qualidade da água para consumo são regulados pelo Conselho Nacional do Meio Ambiente
(Conama), entre outros órgãos reguladores. Na Resolução nº 357/2005 do Conama, em relação
ao pH para águas doces, definem-se valores aceitos, como os apresentados no quadro abaixo.

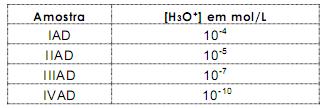
Em um laboratório de análise de águas, obtém-se os seguintes valores de [H3O
+
] para quatro
amostras de águas, identificadas como IAD, IIAD, IIIAD e IVAD.

Em relação à qualidade da água, a amostra adequada para consumo humano é a
O pH é um dos parâmetros da qualidade da água doce para consumo. Os valo res dos parâmetros
da qualidade da água para consumo são regulados pelo Conselho Nacional do Meio Ambiente
(Conama), entre outros órgãos reguladores. Na Resolução nº 357/2005 do Conama, em relação
ao pH para águas doces, definem-se valores aceitos, como os apresentados no quadro abaixo.

Em um laboratório de análise de águas, obtém-se os seguintes valores de [H3O
+
] para quatro
amostras de águas, identificadas como IAD, IIAD, IIIAD e IVAD.

Em relação à qualidade da água, a amostra adequada para consumo humano é a
A
IIIAD.
B
IIAD.
C
IVAD.
D
IAD.