2c8be9e2-b9
UNB 2023 - Química - Transformações Químicas e Energia
Embora o metano seja largamente utilizado como insumo químico pela indústria, a maior parte de sua produção mundial é empregada como combustível. Em comparação aos derivados de petróleo líquidos, como a gasolina e o óleo diesel, o metano propicia uma queima mais “limpa”, com menor emissão de poluentes como benzeno, SO2, CO, NO e material particulado. Além disso, apresenta razão H/C mais elevada, o que resulta em menor emissão de CO2 para uma mesma quantidade de energia gerada.
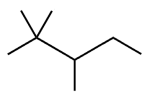
A partir do texto precedente e considerando que as entalpias de combustão do metano e do 2,2,4-trimetilpentano sejam respectivamente iguais a 890 kJ/mol e 5.464 kJ/mol, julgue o item subsequente.
A eventual substituição do 2,2,4-trimetilpentano por metano
como combustível, admitindo-se combustão completa,
permitiria uma redução superior a 20% na quantidade de
CO2 liberada para a mesma quantidade de energia gerada.
Embora o metano seja largamente utilizado como insumo químico pela indústria, a maior parte de sua produção mundial é empregada como combustível. Em comparação aos derivados de petróleo líquidos, como a gasolina e o óleo diesel, o metano propicia uma queima mais “limpa”, com menor emissão de poluentes como benzeno, SO2, CO, NO e material particulado. Além disso, apresenta razão H/C mais elevada, o que resulta em menor emissão de CO2 para uma mesma quantidade de energia gerada.
A partir do texto precedente e considerando que as entalpias de combustão do metano e do 2,2,4-trimetilpentano sejam respectivamente iguais a 890 kJ/mol e 5.464 kJ/mol, julgue o item subsequente.
A eventual substituição do 2,2,4-trimetilpentano por metano
como combustível, admitindo-se combustão completa,
permitiria uma redução superior a 20% na quantidade de
CO2 liberada para a mesma quantidade de energia gerada.
C
Certo
E
Errado