Isomeria Plana: Função, Cadeia e Posição
Publicado em: 18/10/2023A fórmula molecular dos compostos químicos é uma informação muito importante na química, pois informa a quantidade exata de cada tipo de átomo pertencente a molécula. Contudo, é a fórmula estrutural que identifica como os átomos estão ligados para formação das moléculas, pois essa configuração é fundamental para a determinação da propriedade químicas e físicas dos compostos. Desse modo, chama-se de isomeria o fenômeno em que dois compostos orgânicos apresentam a mesma fórmula molecular, mas apresentam diferente fórmula estrutural e consequentemente distintas características. A isomeria plana é o caso particular de isomeria em que é possível identificar a diferença entre os isômeros através na análise da sua estrutura plana. Salienta-se que a isomeria plana é um assunto muito recorrente na prova do Enem, o que faz com que os candidatos precisem compreender bem as suas características e diferenças.
Isomeria plana de função
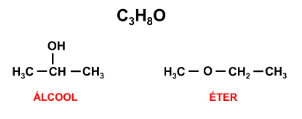
As funções químicas são classes de compostos orgânicos que apresentam uma parte em comum chamada de grupo funcional. Desse modo, a isomeria plana de função corresponde a relação entre duas substâncias que possuem a mesma fórmula molecular, com fórmula estrutural e funções distintas. Como esperado, cada função orgânica apresenta suas características bem definidas, assim os isômeros de função apresentam características diferentes. Um dos casos mais comuns de isomeria plana de função ocorre entre álcoois e ésteres como visto a seguir:
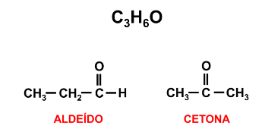
As funções aldeído e cetona também podem formar pares de isômeros, pois ambas são classificados como compostos oxigenados. Um bom exemplo são o propanal e a propanona que apresentam a mesma quantidade de átomos de carbono, hidrogênio e oxigênio, entretanto possuem modos de ligação diferentes.
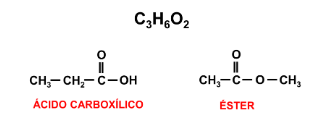
As funções ácido carboxílico e ésteres também formam pares de isômeros apresentando tais como o ácido propanóico e o etanoato de metila.
Isomeria plana de cadeia
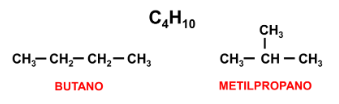
Outra classe de isômeros bastante conhecidos são os isômeros planos de cadeia que se caracterizam por ser espécies com a mesma fórmula molecular, entretanto a estrutura das cadeias carbônicas é diferente. Um exemplo de par de isômeros de cadeia é o propano e o metilpropano, visto que ambos compostos apresentam a mesma quantidade de carbono e hidrogênio, contudo o propano apresenta uma cadeia normal enquanto o metilpropano apresenta sua cadeia ramificada.
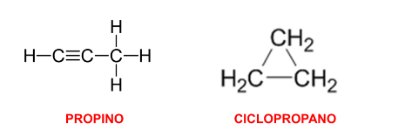
Outro tipo de isomeria de cadeia ocorre quando um composto apresenta cadeia aberta e o outro apresenta cadeia cíclica. Um bom exemplo desse tipo de isomeria ocorre entre o propino (hidrocarboneto com a presença de uma ligação tripla) e o ciclopropano (hidrocarboneto de cadeia fechada). Observa-se que os isômeros de cadeias apresentam a mesma função orgânica, modificando somente o tipo de cadeia e suas características físicas e químicas.
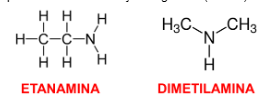
Existem ainda compostos com cadeia homogênea e heterogênea que apresentam isomeria de cadeia, como na etanamida (CH3 - CH2 - NH3) que possui uma cadeia homogênea, tendo em vista que o nitrogênio não se encontra inserida no meio da cadeia carbônica e a dimetilamina (CH3 - NH2 - CH3) que possui cadeia heterogênea, pois o nitrogênio está localizado no meio da cadeia carbônica. Salienta-se que ambos os compostos fazem parte da mesma função orgânica (amina).
Isomeria plana de posição
Os isômeros de posição se caracterizam por possuírem a mesma fórmula estrutural, entretanto possuem em sua constituição mudanças na posição do heteroátomos, das ramificações ou dos grupos funcionais, apresentando assim características distintas. Quanto a posição do heteroátomo que consiste em um átomo diferente de carbono e hidrogênio no meio da cadeia carbônica, podemos identificar inúmeros exemplos tais como o Etoxietano (CH3 - CH2 - O - CH2 - CH3) e Metóxipropano (CH3 - O - CH2 - CH2 - CH3). Observa-se que ambos os compostos apresentam a mesma função e fórmula molecular, entretanto a posição do oxigênio é diferente, gerando desse modo diferença nas características dos compostos.
Existem também isômeros que se diferenciam somente pelo posicionamento da ramificação na cadeia carbônica, o que pode ser facilmente verificado analisando a fórmula estrutural do 2-metil-pentano e do 3-metil-pentano.
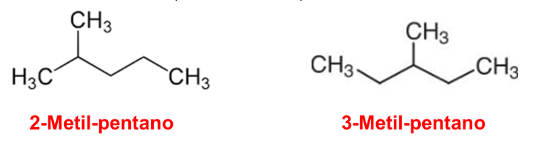
Visualmente pode parecer que a mudança de posição da ramificação pouco interfere nas propriedades, contudo ao se analisar as características de ambos compostos observam-se distinções.
A posição do grupo funcional também afeta a estrutura dos compostos orgânicos gerando isômero de posição como no propan-1-ol e do propan-2-ol.
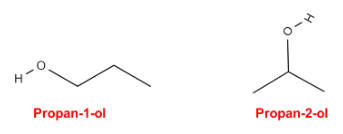
Ao verificar sua fórmula estrutural, é possível inferir que a mudança na posição da hidroxila desses átomos ocasiona mudanças drásticas nas características de cada uma das substâncias.
Isomeria Plana - Função, Cadeia e Posição no Enem
A isomeria plana no Enem já foi em diferentes edições trazendo em muitos casos uma aplicação cotidiana dos isômeros e suas distintas propriedades, fazendo com que os candidatos compreendam o que é isomeria plana, além de analisar e diferenciar a isomeria plana de função, de cadeia e de posição. O domínio dessa temática dentro da matéria de química orgânica é de suma importante para um com desempenho na prova do Enem.
(ENEM 2012) Motores a combustão interna apresentam melhor rendimento quando podem ser adotadas taxas de compressão mais altas nas suas câmaras de combustão, sem que o combustível sofra ignição espontânea. Combustíveis com maiores índices de resistência à compressão, ou seja, maior octanagem, estão associados a compostos com cadeias carbônicas menores, com maior número de ramificações e com ramificações mais afastadas das extremidades da cadeia. Adota-se como valor padrão de 100% de octanagem o isômero do octano mais resistente à compressão.
Com base nas informações do texto, qual dentre os isômeros seguintes seria esse composto?
a) n-octano.
b) 2,4-dimetil-hexano.
c) 2-metil-heptano.
d) 2,5-dimetil-hexano.
e) 2,2,4-trimetilpentano.